云南白药药品事业部 云南昆明 650500
【摘要】 目的:建立生产系统中冰片粉碎设备清洁验证分析方法及取样方法。方法:采用GC,聚乙二醇20000(PEG-20M)为固定相,涂布浓度为10%。进样口温度200℃,检测器温度260℃,柱温为140℃;进样量为1ul。理论板数按龙脑峰计算应不低于2000。结果:冰片中的龙脑(C10H18O)在浓度为 50%~150%范围内线性良好,r=0.9998。平均加样回收率为98.0%,采用棉签擦拭法取样,钢板取样回收率可达84.2%。结论:该方法简便、灵敏度高、专属性强、干扰性小,可作为冰片粉碎设备清洁后药品残留量的检验分析方法。
【关键词】冰片 清洁验证 GC 残留量
1 仪器与试药
1.1 仪器 气相色谱仪:岛津2010气相色谱仪系统,配有气路系统、自动进样器、柱温箱及FID检测器,数据处理系统。色谱柱:聚乙二醇20000(PEG一20M)为固定相,涂布浓度为10%。 天平:SARTORIUS BP211D.
1.2试药及材料 高纯氢(99.999 %)、高纯氮(99.999 %) 、无水空气,乙酸乙酯(AR),TOC棉签,不锈钢板(4×4×25cm2)等。
1.3对照品:龙脑(C10H18O)(中国药品生物制品检定所提供,批号:1108881-201107)
2 方法与结果
2.1色谱条件与系统适用性试验 进样口温度200℃,检测器温度260℃,柱温为140℃;进样量为1ul。理论板数按龙脑峰计算应不低于2000。
2.2龙脑对照品储备液的制备
精密称取龙脑对照品3.36 mg、4.13 mg,分别置100ml容量瓶中,加乙酸乙酯适量使溶解,再用乙酸乙酯稀释至刻度,摇匀,即得33.6ug/ml、41.3ug/ml的(1)、(2)双对照品储备液。
2.3 供试品储备液的制备
精密称取冰片粉(批号:Y1203005,含龙脑58.7%)6.709mg,置100ml容量瓶中,加乙酸乙酯适量,使溶解,再用乙酸乙酯稀释至刻度,摇匀,即得67.09ug/ml(含龙脑39.38ug/ml)的供试品储备液。
2.4 系统适用性
2.4.1精密量取龙脑对照品储备液(1)、(2)1ml,分别置10ml容量瓶中,用乙酸乙酯稀释至刻度,制得浓度为3.36ug/ml、4.13ug/ml的双对照品溶液。分别取两份对照品溶液和供试品溶液1ul,注入GC色谱仪,记录色谱图。
2.4.2结果 浓度为3.36ug/ml、4.13ug/ml的双对照品溶液分离度R均为8.2,大于1.5, 拖尾因
子分别为1.03和1.05,在0.95~1.05之间,理论踏板数分别为398721、428949,大于2000,均符合规定。表明该系统适用性试验符合规定要求。
2.5 定量限和检测限
根据《药品GMP验证指南》(2010年修订)对清洁验证化学检验方法的规定,残留限度10ppm(0.3466ug/cm2)应达到定量限(≥1000倍峰高),定量要求低于通常仪器分析的要求;残留限度10ppm/10(0.3466ug/cm2/10)应达到检测限(≥100倍峰高),检测限要求低于定量限要求。
2.5.1 分别精密量取龙脑对照品储备液1ml,置10ml和100ml容量瓶中,用乙酸乙酯稀释至刻度,制得浓度为3.36ug/ml和0.336ug/ml的对照品溶液。
2.5.2 精密量取龙脑对照品溶液1ul,注入气相色谱仪,记录色谱图。
2.5.3结果 见表1;
表1 龙脑(C10H18O)定量限/检测限结果
| 对照品浓度 | 峰高 | 平均峰高 | 平均峰面积 | 峰高RSD% | 是否符合规定 |
| 3.36 (ug/ml) | 1724 1714 | 1719 | 5317 | 0.4% | 符合规定 |
| 0.336 (ug/ml) | 191 187 | 189 | 570 | 1.5 | 符合规定 |
2.5.4 结论 定量限/检测限符合标准规定
2.6 专属性
2.6.1阴性对照:在不锈钢板上选择4块面积为25cm2的方块,然后分别将4支棉签放入盛有75%乙醇的试剂瓶中湿润,按取样方法取样图3,将棉签头剪下放入广口瓶中,精密加入10ml乙酸乙酯,超声10分钟 ,过滤,即得。
2.6.2 精密量取龙脑对照品储备液(1)1ml,置10ml容量瓶中,用乙酸乙酯稀释至刻度,制得浓度为3.36ug/ml的对照品溶液。
2.6.3 精密称冰片供试品储备液1ml,置10ml容量瓶中,用乙酸乙酯稀释至刻度,制得浓度为6.709ug/ml的供试品溶液。
2.6.4分别取阴性对照品溶液、阳性对照品溶液和供试品溶液1ul,注入液相色谱仪,记录色谱图。
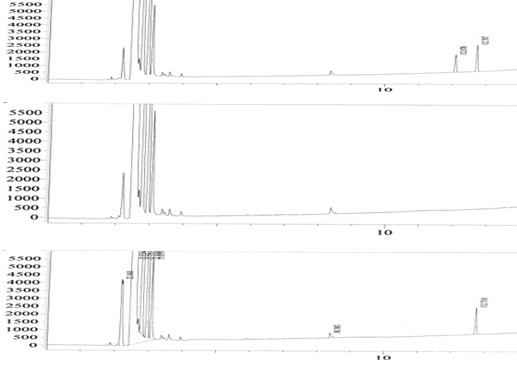
图1从上到下分别是供试品图谱、阴性对照图谱、阳性对照图谱。
2.6.5结论 阴性对照无龙脑 GC色谱峰(R为/,峰面积为0),供试品溶液GC色谱中有与对照品溶液GC色谱峰保留时间一致的色谱峰。说明气相色谱法对冰片中的龙脑专属性强。
2.7 线性关系
2.7.1 分别精密量取龙脑对照品储备液(1)0.3ml、0.5ml、0.8ml、1.0ml、1.2ml、1.5ml、1.8ml,置10ml容量瓶中,加用乙酸乙酯稀释至刻度,摇匀,即得浓度为1.008ug/ml、1.68ug/ml、2.688ug/ml、3.36ug/ml、4.032ug/ml、5.04ug/ml、6.048ug/ml的溶液。分别取不同浓度的对照品溶液 1ul,注入GC色谱仪,记录色谱图。以对照品中龙脑峰面积作为纵坐标,浓度作为横坐标作线性图,列出回归方程和相关系数。
2.7.2结果见图2:
图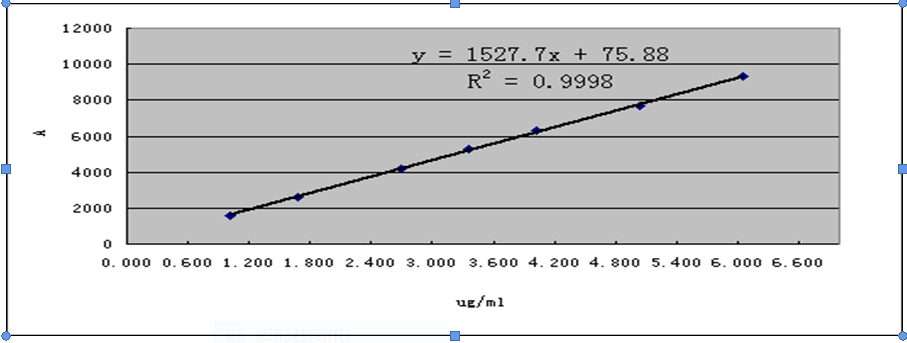 2 龙脑(C10H18O)气相线性回归
2 龙脑(C10H18O)气相线性回归
2.7.3结论 龙脑对照品在浓度为 50%~150%范围内线性良好,相关系数0.9998符合规定要求。线性回归方程为 y=1527.7x + 75.88 ,R2= 0.9998 。
2.8精密度
2.8.1精密量取龙脑对照品储备液(1)、(2)1ml,分别置10ml容量瓶中,用乙酸乙酯稀释至刻度,制得浓度为3.36ug/ml、4.13ug/ml的对照品溶液。
2.8.2 精密量取对照品溶液1ul,注入GC色谱仪,重复测定6次,记录色谱图,进行相对标准偏差分析。
2.8.3 结论 测得RSD均为0.3% ,标准规定相对标准偏差 RSD%应≤3%。表明龙脑对照品溶液气相测定,精密度符合标准规定。
2.9 准确度
2.9.1 精密量取龙脑对照品储备液1ml、0.5ml分别置于10ml的容量瓶中,用乙酸乙酯稀释至刻度,即得std1 3.36ug/ml和std2 2.065ug/ml的对照品溶液。
2.9.2 分别精密量取std1 的照品溶液0.3ml、0.5ml、0.7ml置HPLC进样瓶中,自然晾干,再精密量取std2的对照品溶液1ml置以上HPLC瓶中,混匀,取1ul注入GC色谱仪,记录色谱图,计算回收率(P%)值,以及回收率的相对标准偏差 RSD。
2.9.3 回收率计算公式 P=(C-A)/B×100%
A加入龙脑std1对照品的量;B加入龙脑std2对照品的量;C 混合对照品溶液中龙脑的实测量。
2.9.4 结果 三水平80%、100%、120%的加样回收率分别为97.7%、97.5%、98.9%,平均值为98.0%, RSD为0.86% .
2.9.5 结论 表明三个不同浓度水平的对照品溶液加样回收率P均大于75%,加样回收率的相对标准偏差RSD大于10%,即本品具有良好的回收率。
2.10样品溶液稳定性
2.10.1 分别取对照品溶液和第0h、6h、12h、24h、36h、48h的供试品溶液1ul,注GC色谱仪,记录色谱图。
2.10.2结果 环境温度为25.4-25.8℃,相对湿度为54%-58%,龙脑含量测定0h、6h、12h、24h、36h、48h分别为 3.63034、3.64675、3.64959、3.64959 ug/ml。龙脑含量的相对标准偏差为0.2%,小于5% 。
2.10.3结论 表明冰片样品溶液在常温、常湿,未避光密封保存下,经48h放置,其性状不变,说明该样品溶液稳定性较好 。
3取样方法验证
3.1棉签擦拭法取样[3]
根据取样部位大小,分别将4支棉签分别放入盛有乙醇的瓶中湿润,并将其靠在瓶口上挤压以挤去多余的乙醇,每支棉签擦拭取样25cm2,共擦拭取样100cm2(应避免与微生物检测取样点重复)。擦拭时平擦和竖擦,尽量擦完全。擦完将棉签头剪下放回广口瓶中,贴上标签,注明样品名称、样品编号、取样人及取样日期。
3.2 回收率溶液的制备
在不锈钢板上选择4块面积为25cm2的方块,分别取供试品储备液 0.25ml均匀涂布于钢板方块上,在环境温度下干燥过夜;然后分别将4支棉签放入盛有75%的试剂瓶中湿润,按取样方法取样,擦拭完后,将棉签头剪下放入广口瓶中,精密加入10ml乙酸乙酯,超声10分钟使活性成分溶解,过滤,即得。
3.2.1分别量取浓度为3.36ug/ml的对照品溶液、 供试品溶液、回收率溶液各10ul,注入气相色谱仪,记录色谱图,并计算回收率(Q)。
3.2.2
测定结果 见表2。
表2 取样回收率及其相对标准偏差
| 钢板 样品 | 1 (4×25cm2) | 2 (4×25cm2) | 3 (4×25cm2) |
| Cc(ug) | 3.09319 | 2.96190 | 3.12160 |
| Cs(ug) | 3.63034 | 3.63034 | 3.63034 |
| 回收率Q(%) | 85.2% | 81.5% | 85.9% |
| 平均回收率(%) | 84.2% | ||
| 回收率RSD(%) | 2.81% | ||
回收率计算公式Q=Cc/CS×100%
(Q:取样回收率;Cc:供试品溶液钢板擦拭龙脑(C10H18O)的回收量;Cs:供试品溶液中龙脑(C10H18O)的量)
3.2.3 回收率Q应≥50%;相对标准偏差RSD应≤20%;
3.2.4 结论 平均回收率为84.2%>50%以及回收率的相对标准偏差为2.81%<20%,证明了按既定的取样方法取样,能确保取样过程的回收率和重现性达到预定要求
4 讨论
4.1 冰片分天然冰片和合成冰片两种,目前药用的主要为合成冰片,外观性状为无色透明或白色半透明的片状松脆结晶;气清香,味辛、凉;本品在乙醇、氯仿、汽油或乙醚中易溶,在水中几乎不溶,本文钢板取样回收率验证中采用了乙醇做擦拭溶剂,结果平均取样回收率达84.2%,通过理论和试验证明乙醇做清洗剂即可消毒又达到预期的清洗目的;因此在生产设备清洁过程中建议采用乙醇做为清洗剂。
4.2 冰片含量测定的法定分析方法为气相色谱法,本文以冰片残留限度为检测限度,通过对气相色谱法的定量限、专属性、精密度、准确度、线性/范围、样品溶液稳定性、系统适用性等参数的验证,其结果均符合规定要求,因此冰片粉生产设备清洁验证的清洁质量控制检验方法确定为气相色谱测定法。
4.3 通过冰片生产设备分析方法的研究,冰片粉碎设备清洁验证的残留限度(棉签擦拭法取样)按龙脑的百万分之十(10ppm)计算,既符合GC分析方法的参数要求,又达到设备的清洁质量控制,因此表面残留限度确定为龙脑的百万分之十(10ppm)即0.3466ug/cm2,设备按既定程序清洗,清洁样品龙脑测定量应大于0.3466ug/cm2。
4.4 清洁验证取样方法—棉签擦拭法确定为每只棉签擦拭25cm2,每个取样点擦拭100cm2,共需4只棉签,4只棉签用10ml乙酸乙酯做溶剂 ;超声10分钟,微孔滤膜过滤,上机测定。
参考文献
[1]国家药典委员会.中华人民共和国药典2015版(一部)[S] [S]北京,国家药典委员会编,中国医药科技出版社,2015.6。
[2]黄卫东 冰片的研究进展[J] 中国药业.2008(4):64
[3]刘华本,陈晓平,范愿军.制药设备清洁验证的关键步骤[J].医药导报,2009,
28(5):681-683.
[4]邓海根. 制药企业GMP管理实用指南[M ].北京:中国计量出版社, 2000.
[5]国家食品药品监督管理局药品认证管理中心.药品GMP指南[M].北京:中国医药科技出版社,2010:181-191.
作者简介:危菊芬(1982~)女,大学本科,2006年毕业于云南中医学院中药系。工程师,执业药师, 任职于云南白药集团股份有限公司,曾从事药品质量控制,目前主要从事药品生产管理。
5