昆明同仁医院 云南省 昆明市 650000
【摘要】目的:探析2型糖尿病(DPN)患者血尿酸与周围神经病变的相关性。方法:选取本院于2017年01月~2019年01月收治的80例2型糖尿病患者,根据尤为DPN分为对照组(单纯2型糖尿病,31例)与观察组(合并周围神经病变,49例),对比两组分析两组患者的SAU水平及周围神经病变多因素。结果:观察组SUA水平显著高于对照组(P<0.05);SUA是DPN发生、发展的独立高危因素。结论:SUA是DPN发生、发展的独立危险因素,有效控制SUA水平对减少或抑制DPN的发生、发展、发挥起到实质性的影响作用,指标预测还需循证医学加以研究。
【关键词】2型糖尿病;血尿酸;周围神经病变;相关性
临床已有大量研究证实,血尿酸(SUA)与SM的重要组成部分具有正相关联系,可与高血压、IR、肥胖及高脂血症等因素发挥协同效应,促进T2DM、DN等并发症的发生与发展[1]。而目前对于SUA是否可作为DPN发生、进展变化的独立危险因素、两者间连带严重程度研究相对较少。鉴于此,本研究为探析2型糖尿病(DPN)患者血尿酸与周围神经病变的相关性,报告如下:
1 资料与方法
一般资料
选取本院于2017年01月~2019年01月收治的80例2型糖尿病患者,根据尤为DPN分为对照组(单纯2型糖尿病,31例)与观察组(合并周围神经病变,49例),男57例,率23例,年龄44~71(57.4±12.6)岁,患者的一般资料不具统计学意义(P>0.05),临床可对比。
1.2方法
患者空腹>10h,采集患者晨起肘静脉血,常规检测中的空腹血糖( FBG)、血尿酸(SUA)、总胆固醇(TC)、三酰甘油(TG)、高密度脂蛋白胆固醇(HDL-C)、低密度脂蛋白胆固醇(LDL-C)、C-反应蛋白(CRP)、血肌酐(SCr)等指标水平。
1.3统计学方法
将数据纳入SPSS22.0软件中分析,计量资料比较采用t检验,并以(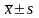 )表示,率计数资料采用χ2检验,并以率(%)表示,(P<0.05)为差异显著,有统计学意义。
)表示,率计数资料采用χ2检验,并以率(%)表示,(P<0.05)为差异显著,有统计学意义。
2 结果
2.1 2型糖尿病周围神经病变多因素分析
表1 2型糖尿病周围神经病变多因素分析[n,(%)]
因素 | 回归系数 | 标准误 | Waldχ2 | P | OR | 95%CI |
SUA | 0.511 | 0.255 | 5.014 | 0.015 | 2.011 | 1.254~4.381 |
SCr | 0.435 | 0.198 | 4.279 | 0.033 | 1.917 | 1.049~4.957 |
病程 | 0.612 | 0.389 | 5.275 | 0.026 | 1.879 | 1.201~6.142 |
TC | 0.501 | 0.271 | 9.443 | 0.003 | 2.927 | 1.381~6.837 |
2.2 对比两组患者的SUA水平
观察组SUA水平为( 381. 29±40. 42) μmol /L,显著高于对照组的SUA水平为( 317. 58±25. 41) μmol /L,差异具统计学意义(P<0.05) (t=8.656,P=0.0001)。
3.讨论
DPN是糖尿病常见并发症之一,其致病成因与发病机制现阶段尚不具统一标准定论。目前,炎症、氧化应激反应对其发生、发展产生的作用备受关注。相关研究认为,机体长时间处于高血糖状态,引发微血管病变,可作为DPN发病的的重要作用机制[2]。
而一项荟萃研究分析表明,高尿酸血症与DPN的风险增加具有直接连带性,DPN患者的SUA水平显著高于常人[3]。但SUA是否可作为DPN发生、进展变化的独立危险因素、两者间连带严重程度研究相对较少,本文研究即主要探析SUA水平与DPN的相关性。
尿酸( UA) 通过促进血管平滑肌细胞增殖,刺激血管壁,引发血管收缩,阻碍内皮细胞释放一氧化氮( NO) 等作用,造成血管功能障碍,导致组织缺血,进而损伤周围神经功能。而血尿酸(SUA)在正常水平下,其抗氧化特性可保护机体,但一旦超出正常水平,可迅速转为促氧化特性,发展为致病因素。患上高尿酸血症,微结晶可轻易析出且凝积于血管壁,产生局部炎性反应进而损害血管内皮。
血尿酸水平的异常上升参与DPN的发生、发展,但细致的参与机制现阶段存在较多异声,相对较统一的结论认为:机体处于高尿酸水平状态下,可激活多元醇通路,诱发血中大量沉积果糖、山梨醇,导致磷酸肌醇代谢、脂肪酸代谢水平升高,受到蛋白激酶C通道激活反应及其他连带因素的联合作用机制下参与DPN的发生发展及发挥。相关研究表明,糖尿病、IL-6、UA均是影响周围神经系统神经传导速率( NCV) 、效果的关键且独立预测因素[4]。即可说明SUA作为天然抗氧化剂之一,对部分多系统硬化、帕金森病等神经系统疾病中可发挥较强的抗氧化作用,保护神经损害活动。
本次研究结果显示,观察组SUA水平显著高于对照组,差异具统计学意义(P<0.05);Logistic回归分析结果显示,SUA水平是DPN发生、发展的独立危险因素。即提示血尿酸水平与DPN的发生发展具有正相关的连带性,分析其可能机制如下:首先,尿酸是体内嘌呤代谢物,具有强大的促氧化剂、抗炎作用,可通过直接或间接作用参与并促进氧化应激反应,进而损伤周围神经功能;SUA可引发胰岛素抵抗,而高胰岛素状态下可阻碍内皮源性一氧化氮的生成,导致血管内皮细胞收缩;尿酸盐是一种炎性物质,SUA水平一旦异常上升,尿酸盐大量凝聚于血管壁,产生炎症反应,损伤血管内皮,进而激活补体及血小板,发生凝血作用,于血管局部中产生血栓,降低细胞及组织血供;SUA可增强脂质过氧化及低密度脂蛋白氧化反应,同步增值且增加氧自由基,提升炎症反应,进而损伤周围神经功能。
综合所述,SUA是DPN发生、发展的独立危险因素,有效控制SUA水平对减少或抑制DPN的发生、发展、发挥起到实质性的影响作用,指标预测还需循证医学加以研究。
参考文献
[1] Vasilios G. Athyros. Uric acid, chronic kidney disease and type 2 diabetes: A cluster of vascular risk factors[J]. Journal of Diabetes and Its Complications,2014,28(2).
[2] 万芳.糖化血红蛋白、C肽与2型糖尿病周围神经病变的相关性分析[J].中国现代医生,2018,56(29):27-29.
[3] YU S,CHEN Y,HOU X,et al. Serum Uric Acid Levels and Diabetic Peripheral Neuropathy in Type 2 Diabetes:a Systematic Review and Meta- analysis[J].Mol Neurobiol,2016.53(2):1 045-1 051.
[4] Di Iorio Angelo,Cherubini Antonio,Volpato Stefano,et al. Markers of inflammation, vitamin E and peripheral nervous system function: the InCHIANTI study.[J]. Neurobiology of aging,2006,27(9).