贵黔国际总医院,贵州贵阳 550001
[摘要]目的:基于美国 FDA 不良事件报告系统(FAERS),对吡格列酮药物相关膀胱癌不良事件进行数据挖掘,为临床安全使用提供参考。方法:下载 2004Q1 至 2019Q4 共 64个季度的 FAERS 数据,经过MedEx 药品名称标准化、MedDRA 不良事件系统分类等数据清洗后,提取吡格列酮不良事件数据,采用报告比值比法(ROR)和比例报告比值法(PRR)进行信号检测。结果:共提取到吡格列酮不良事件报告记录14671条,吡格列酮相关膀胱癌事件报告9570条(65.2%),其中,各种恶性膀胱肿瘤的ROR=3443.58、PRR=1197.96;膀胱癌 0 期ROR=270.75、PRR=270.43;膀胱癌 I 期ROR=337.44、PRR=337.08;膀胱癌 II 期ROR=367.42、PRR=366.82;膀胱癌 III 期ROR=440.37、PRR=439.71,膀胱癌 IV 期ROR=240.04、PRR=239.84;未指定分期的膀胱癌ROR=3470.36、PRR=1217.68。结论:长期使用该药的病患或高风险人群应定期检查并重视潜在的风险。
[关键词]吡格列酮;膀胱癌;不良事件;数据挖掘
Data mining of pioglitazone associated bladder cancer based on FAERS
CHEN Yunxi (Guiqian International General Hospital, Guiyang 550001, China)
[Abstract] OBJECTIVE: Based on FDA Adverse Event Reporting System (FAERS), data mining of pioglitazone related adverse events was conducted, so as to provide reference for clinical safe use.METHODS: FAERS data of 60 quarters were downloaded from Q1, 2004 to Q4, 2018. After data cleaning, such as Medex drug name standardization and MedDRA adverse event classification system, the adverse event data of piogritazone were extracted, and signal detection was performed by RORs and PRR methods.RESULTS: A total of 14,671 adverse event records of pioglitazone were collected, and 9570 (65.2%) pioglitazone-related bladder cancer event reports were collected. Among them, ROR3443.58 and PRR1197.96 of various malignant bladder tumors were detected.ROR270.75 and PRR270.43 in stage 0 bladder cancer;ROR337.44 and PRR337.08 in stage I bladder cancer;Bladder cancer stage II ROR367.42, PRR366.82;ROR440.37 and PRR439.71 in stage III bladder cancer and ROR240.04 and PRR239.84 in stage IV bladder cancer;Bladder cancer ROR3470.36, PRR1217.68 without specified stage.Conclusions: Patients who have been using this drug for a long time or those at high risk should be checked regularly and be aware of the potential risks.
[Key words] pioglitazone;Bladder cancer;Adverse events;Data mining
吡格列酮是2型糖尿病的治疗药物,是一种较有争议的噻唑烷二酮类药物[1]。它的作用机制是通过特异性激活抗转录因子过氧化物酶体增值物活化受体y,以增加外周组织和肝脏对胰岛素的敏感性,降低机体的胰岛素抵抗。该药有效的降低了心血管事件的发生风险,但是不良反应也在陆续报到。
吡格列酮于1999年首次上市以来,膀胱癌的风险一直是药品监督管理局(FDA)备受关注的问题。2010年9月FDA基于一项10年流行病学研究的中期结果,提醒公众吡格列酮潜在膀胱癌风险。随即,2011年8月,说明书中包含吡格列酮药物的警告这一风险信息[2]。法国一项 PROactive 研究[3]也说明了两者存在一定的风险具有关联性。2011年6月法国宣布暂停使用含吡格列酮的药物[4]。我国药品监督管理部门也开展了毗格列酮安全性监测和评估工作,国家食品药品监督管理局发布第42期[5]药品不良反应信息通报,提醒医务人员和患者关注毗格列酮可能引起膀胧癌的风险。
本文将通过FDA不良事件报告系统(FDA Adverse Event Reporting System,FAERS)大数据开展数据挖掘研究,进一步探寻吡格列酮与膀胱癌的关系,评估吡格列酮上市后安全性。
1、数据与方法
1.1数据来源
1.1.1药品不良事件源数据:数据来源于公开免费的FAERS数据[6]。本研究下载 2004Q1 至 2019Q4,共 64 个季度的数据,选择个人信息记录(DEMO)、不良事件记录(REAC)、药物使用记录(DRUG)和治疗记录(THER)数据表进行后续分析。
1.1.2药品名称标准化系统:采用美国 Vanderbilt 大学开发的 Medex_UIMA_1.3.7 系统进行药品名称标准化和RxNorm 编码(RxCUI)[7]。
1.1.3药品不良事件编码系统:FAERS 不良事件数据采用《ICH 国际医学用语词典》(Medical Dictionary for Regularly Activities, MedDRA)首选语(preferred terms, PT),下载 MedDRA 21.1 版,用于首选语(PT)、高位语(high level term, HLT)、高位组语(high level group term, HLGT)、系统器官分类(system organ class, SOC)编码和语言汉化[8]。本文基于HLT和PT两个层级进行分析。
1.2数据处理
1.2.1数据清洗:根据 FAERS 说明文件去除 DEMO 表重复报告。采用 Medex_UIMA_1.3.7 系统对 DRUG 表中药品名称进行标准化处理。采用 MedDRA 21.1 对REAC 表中不良事件名称进行系统映射和汉化处理。
1.2.2数据提取:查询标准化 DRUG 表中 pioglitazone作为首要怀疑(primary suspect, PS)对象的记录作为目标药品。基于MedDRA分类,查询 REAC 表中吡格列酮相关的“各种恶性膀胱肿瘤”(HLT code=10005013)项下的所有PT事件(含32个PTs)。
1.2.3数据分析:不良事件信号检测采用报告比值比法(reporting odds ratio, ROR)和比例报告比值法(proportional reporting ratio, PRR)。ROR 法双侧检验 95%CI 下限≥1 提示信号, PRR 法报告数≥3,PRR≥2 且 χ2≥4 提示信号[9]。统计分析采用 SPSS 20.0 软件和 Microsof Excel 2016 软件。
2、结果
2.1不良事件报告情况
经过数据清洗,得到药品不良事件报告11,450,530例,其中吡格列酮首要怀疑相关报告14671条,其中吡格列酮相关膀胱癌事件报告 9570例(65.2%)。报告基本信息参见表 1,图1。
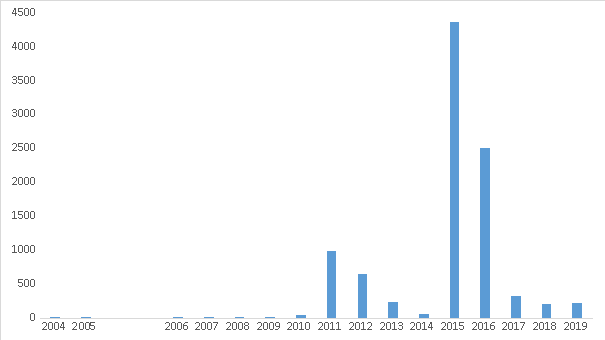
图1 FAERS数据库中年度吡格列酮相关膀胱癌事件病例报告
Figure 1 Annual reports of pioglitazone-associated bladder cancer events in FAERS database
2.2信号检测结果
经 ROR 和 PRR 法信号检测,吡格列酮在HLT水平上“各种恶性膀胱肿瘤”检出信号。在PT水平,将膀胱癌按分期分类,0至IV期以及未指定分期的膀胱癌经两种方法检测后均有明显的信号提示。
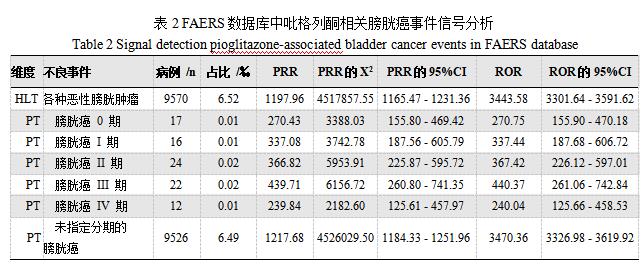
2.3事件发生时间
纳入报告中9570例中有1762例报告了开始药物治疗至不良事件发生的时间,统计结果显示“各种恶性膀胱肿瘤”事件发生中位时间为44.22个月,膀胱癌I至IV期发生中位时间整体呈上升趋势。
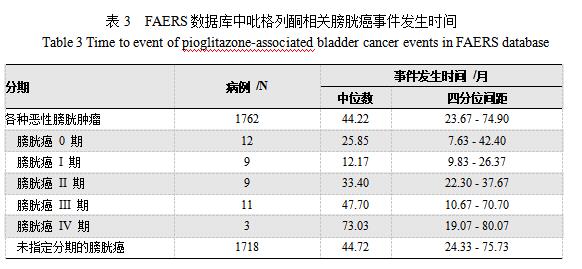
3、讨论
通过 FAERS 数据挖掘发现,吡格列酮相关膀胱癌事件信号强烈。从报告时间可见,2011年吡格列酮相关的膀胱癌事件报告突起,2015年达高峰。从报告国家来看,北美洲报告数据远超其他国家,吡格列酮相关的膀胱癌事件引起各国的重视。此外,风险年龄大多在65-84岁左右,男性占比或高于女性,建议长期口服吡格列酮超过3年左右的老年糖尿病史的男性应重点关注该药安全性。
经 ROR 和 PRR 法信号检测,吡格列酮在各分期的膀胱癌事件上均检出了较强的信号,揭示吡格列酮与膀胱癌事件存在关联性。法国一项 PROactive 研究[3],超过 149 万糖尿病患者,有 15.5 万人服用吡格列酮,结果显示,服用吡格列酮与膀胱癌风险相关(HR 1.22;95 %CI:1.05~1.43),且剂量与效应呈正相关;高剂量增加膀胱癌的风险 (≥28000mg,HR 1.75;95%CI:1.22~2.5),服用更长时间的患者膀胱癌的风险有所增加(≥24 个月,HR 1.36;95%CI:1.04~1.79)[10]。加拿大医学协会杂志(CMAJ)发表的一项研究指出,2型糖尿病常用药物吡格列酮可增加膀胱癌患病风险[11]。基于这些发现,相关各国都已采取了适当的对应措施。虽然我国截止到2011年8月底没有接收到关于膀胱癌的不良反应报告,国家药品不良反应监测中心特发布药品不良反应信息通报(第42期) 关注吡格列酮的膀胱癌风险,以进一步规范吡格列酮的临床应用,降低其使用风险,保障公众用药安全。
因此,特此呼吁医务人员和患者应该对高风险人群可考虑替代药品进行治疗或者是定期检查;对于长期口服出现血尿、尿频、尿急、排尿疼痛症状应立即就医。需注意的是,由于自发呈报系统的低报漏报特点,可能存在信号低估可能[12]。吡格列酮与膀胱癌的因果关系仍需进一步评估和验证。
参考文献:
[1]Laurent Azoulay assistant professor,Hui Yin statistician,Kristian B Filion assistant professor2,et a1.型糖尿病患者服用吡格列酮的膀胱癌风险 [J]. 中国处方药,2012,10(5): 40-43.
[2] Updated FDA review concludes that use of type 2 diabetes medicine pioglitazone may be linked to an increased risk of bladder cancer,FDA Drug Safety Communication: Updated drug
labels for pioglitazone-containing medicines 2011,August 4.
[3] Colmers I N,Bowker S L,Majumdar S R,et a1.Use of thia-zolidinediones and the risk of bladder cancer among people with type 2 diabetes:a meta- analysis [J].CMAJ,2012,84(12):675- 683.
[4] 国家食品药品监督管理局,中国社区医师[EB/OL].2011年12月2日9版
[5] 国家食品药品监督管理局,关注吡格列酮的膀胱癌风[EB/OL].药品不良反应信息通报,险2011年11月8日(第42期)
[6] FDA Adverse Event Reporting System (FAERS) Quarterly Data Extract Files. 2019; Available from: https://fis.fda.gov/extensions/FPD-QDE-FAERS/FPD-QDE-FAERS.html.
[7] 吴斌, 吴逢波, 罗敏, 等. MedEx在FAERS药品名称标准化中的应用 [J]. 中国医院药学杂志, 2019, 39(19): 80-84.
[8] Tieu C and Breder CD. A Critical Evaluation of Safety Signal Analysis Using Algorithmic Standardised MedDRA Queries [J]. Drug Safety, 2018, 41(12): 1375-1385.
[9] Sakaeda T, Tamon A, Kadoyama K, et al. Data mining of the public version of the FDA Adverse Event Reporting System [J]. Int J Med Sci, 2013, 10(7): 796-803.
[10] 颜淑蓉,吡格列酮的临床安全性评述[J].丽水学院学报,2013,35(2):28-32
[11] CMAJ.112102; published ahead of print July 3, 2012, doi:10.1503/cmaj.112102.
[12]齐欣, 刘德平. 光敏感性降压药物增加唇癌风险[J]. 中国心血管杂志, 2012, 17(5): 376-377.
基金项目编号gzwjkj2020-1-208,项目名称为基于FARES数据的镇静催眠类药物致死风险信号挖掘研究;项目负责人:陈韵西;项目单位:贵黔国际总医院。