临洮县兰生单采血浆有限责任公司, 730502
摘要:目的:探讨抗凝与非抗凝血标本对酶联免疫法(ELISA)检测血清乙肝表面抗原的影响。方法:共纳入500名首次献血浆者作为研究对象,采集血液样本,以随机数字表将其分为参照组(250名,非抗凝血液标本)和研究组(250名,枸橼酸钠抗凝剂的抗凝血液样本),均进行ELISA检测血清乙肝表面抗原,比较两组检测结果。结果:与参照组相比,研究组血液样本的HBV A值更高(P<0.05)。两组血液样本中有5例检测结果不一致,均为抗凝血样本,初检时出现灰区值或者反应性,说明枸橼酸钠抗凝剂会影响ELISA检测血清乙肝表面抗原的结果。二次复检5例标本的结果基本一致,假阳性反应消除。结论:ELISA检测血清乙肝表面抗原时对血液样本进行抗凝血处理会对检测结果造成一定的干扰,需经过复检才能定论最终结果,避免漏查情况发生,从而增加检测结果的准确性。
关键词:抗凝;血标本;酶联免疫法;血清乙肝表面抗原
血液制品是应对危难事故的重要战略物资,当患者出现大出血等情况时血液制品是维持其生命的急救药,我国人口基础大且采血总量较小,因此血液制品资源短缺[1]。献血是目前保障血库充足的重要途径,为了保障献血者的安全以及血液制品的质量,需要对血液标本进行检测。考虑到我国乙肝感染的现状以及原料血浆的特殊性,需要进行血清乙肝表面抗原检测,而检测方法以酶联免疫法较多见。研究显示,ELISA检测结果受到标本、操作、试剂等多方面因素的影响,其中标本的抗凝与非抗凝对检测结果的影响是目前重点研究的项目之一[2]。为了明确抗凝与非抗凝血标本对ELISA检测血清乙肝表面抗原结果是否有影响,现开展如下研究。
资料及方法
1.1实验材料
共纳入500名首次献血浆者作为研究对象,采集血液样本,以随机数字表将其分为参照组(250名,非抗凝血液标本)和研究组(250名,枸橼酸钠抗凝剂的抗凝血液样本)。参照组患者中男性177例、女性73例,年龄22-45(34.34±6.56)岁。研究组患者中男性164例、女性86例,年龄22-47(35.03±6.09)岁。对比两组研究对象年龄、性别等基本资料参数均保持了同质性(P>0.05)。
1.2检测试剂
上海科华生物工程股份有限公司提供的乙肝表面抗原试剂盒,批号202106191;四川绵竹鸿基制药有限公司提供的枸橼酸钠抗凝剂,批号00521026。
1.3样本处理方法
参照组患者血液样本放置于非抗凝管内,研究组血液样本放置于枸橼酸钠抗凝管内。使用离心机(湖南湘仪离心机械有限公司提供)对抗凝与非抗凝血标本进行离心处理(转速3000r/min,时间15分钟),将其放置于深圳爱康全自动酶免分析仪(型号URANUS AE 115)进行加样,检测,检验人员需要严格按照试剂盒以及仪器的说明书操作,包括加样、孵育、洗板以及显色等。所有标本的检测需要有同一位检验人员完成。
1.4统计学分析
数据输入SPSS20.0统计学软件,计数资料采用“例数,率”表示,以χ2检验对比。计量资料以(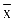 ±s)表示,以t检验。P<0.05为差异有统计学意义。
±s)表示,以t检验。P<0.05为差异有统计学意义。
结果
2.1对比抗凝与非抗凝的HBV A检测结果
与参照组相比,研究组血液样本的HBV A值更高(P<0.05),见表1。
表1 对比抗凝与非抗凝的HBV A检测结果
组别 | A值 |
参照组(n=250) | 0.007±0.006 |
研究组(n=250) | 0.009±0.007 |
t | 3.430 |
P | 0.001 |
2.25份抗凝与非抗凝的HBV A 检测
两组血液样本中有5例检测结果不一致,均为抗凝血样本,初检时出现灰区值或者反应性,说明枸橼酸钠抗凝剂会影响ELISA检测血清乙肝表面抗原的结果。二次复检5例标本的结果基本一致,假阳性反应消除,见表2。
表2 5份抗凝与非抗凝的HBV A 检测结果
样本编号 | 抗凝初检A值 | 抗凝复检A值 | 非抗凝初检A值 | 非抗凝初检A值 | 结果 |
1 | 0.132 | 0.008 | 0.030 | 0.021 | 非反应性 |
2 | 0.278 | 0.012 | 0.017 | 0.010 | 非反应性 |
3 | 0.201 | 0.016 | 0.011 | 0.007 | 非反应性 |
4 | 0.187 | 0.010 | 0.024 | 0.016 | 非反应性 |
5 | 0.156 | 0.006 | 0.018 | 0.009 | 非反应性 |
讨论
随着人们生活水平和健康意识的提升,对各种疾病预防和治疗要求的不断提高,血液制品的需求也在不断增加。而由于血液制品的特殊性,其采集、使用的安全性问题也越来越收到关注,为了保障血液制品的安全性,需要加强血液检测。乙肝是我国较常见的传染性疾病,数据显示,乙型病毒性肝炎感染率已经超过10%,一旦感染,会给患者、家庭以及社会造成较大的负面影响,因此乙肝已经成为重要的公共卫生问题之一[3]。血液检测时乙肝病毒检测结果的准确性会直接影响原料血浆质量、后续血液制品的质量、献血人员的安全以及使用者的安全性。
正常状态下,血液离开人体后会逐渐凝固,而血液经过抗凝混合后可分离出原料血浆,因此抗凝剂在这一过程中具有重要作用。结合学者研究以及临床实践发现,枸橼酸钠抗凝剂毒性更小,可大范围投入使用并获取血液制品[4]。
血液检测是血液制品生产的重要步骤,主要采用ELISA检测,该检测简单快速、结果准确度高且成本低,对设备的要求不高。但研究认为,ELISA检测的影响因素较多,其中抗凝剂对是否对结果产生影响已经成为重点研究内容[5]。本次研究显示,与参照组相比,研究组血液样本的HBV A值更高(P<0.05),说明抗凝剂会在一定程度上影响ELISA检测结果。血液中加入抗凝剂后相当于对血液样本进行稀释,导致乙肝表面抗原数量变少,从而影响检测数据[6]。为了提高ELISA检测结果的准确性,需要对初检结果为反应性的抗凝血样本进行复检才能获取最终结果。本次研究显示,5例检测结果不一致,均为抗凝血样本,初检时出现灰区值或者反应性,二次复检5例标本的结果基本一致,假阳性反应消除。说明枸橼酸钠抗凝剂处理血液样本进行初检,非抗凝以及抗凝的样本均进行一次复检,对灰区或者阳性的标本,其检测结果的准确性较高。
综上所述,ELISA检测血清乙肝表面抗原时对血液样本进行抗凝血处理会对检测结果造成一定的干扰,需经过复检才能定论最终结果,避免漏查情况发生,从而增加检测结果的准确性。
参考文献
[1]孙俊艳, 何成涛, 刘海波,等. 分析前因素对血液乙肝表面抗原检测的影响[J]. 临床检验杂志, 2021, 39(6):470-471,480.
[2]黄洪俊,邹宇,黄红梅. 核酸检测与ELISA检测在无偿献血血液标本乙型肝炎病毒筛查中的应用效果比较[J]. 现代医院,2019,19(12):1852-1853,1856.
[3]王川,程郁菁,雷静,等. 探讨酶联免疫法与胶体金法检测乙肝表面抗原的效果[J]. 生物化工,2018,4(6):72-74.
[4]尤维丹. 乙肝病毒患者HBV-DNA与血清学指标检验结果分析[J]. 医学检验与临床, 2020, 31(2):57-60.
[5]李美苓.酶联免疫吸附法检测乙肝五项结果常见影响因素探讨[J].世界最新医学信息文摘(连续型电子期刊),2018,18(78):141,143.
[6]关秀芬. ECLIA与ELISA检测乙肝病毒血清标志物的效果分析[J]. 中国冶金工业医学杂志, 2020, 37(5):613-614.