大庆市第三医院 163000
【摘要】目的 分析评价丙戊酸钠缓释片联合喹硫平治疗双相情感障碍的安全性和临床疗效。方法 选取本院100例双相情感障碍患者作为本次的研究对象,研究对象选取时间段为2020年5月份到2021年5月份,电脑随机将所有患者均分为参照组(行单一丙戊酸钠缓释片治疗)和研究组(行丙戊酸钠缓释片联合喹硫平治疗),各50例。比较两组不良反应及治疗效果。结果 研究组治疗总有效率明显高于参照组(P<0.05),不良反应发生率明显低于参照组(P<0.05)。结论 二者联合治疗在双相情感障碍中临床效果较好,具有较高的安全性,具有推广价值。
【关键词】丙戊酸钠缓释片;喹硫平;双相情感障碍
[Abstract] Objective To analyze and evaluate the safety and clinical efficacy of sodium valproate sustained-release tablets combined with quetiapine in the treatment of bipolar disorder. Methods 100 patients with bipolar disorder in our hospital were selected as the research object. The research object was selected from May 2020 to may 2021. All patients were randomly pided into reference group (treated with single sodium valproate sustained-release tablets) and research group (treated with sodium valproate sustained-release tablets combined with quetiapine), with 50 cases in each group. The adverse reactions and therapeutic effects of the two groups were compared. Results the total effective rate of the study group was significantly higher than that of the reference group (P < 0.05), and the incidence of adverse reactions was significantly lower than that of the reference group (P < 0.05). Conclusion the combined treatment of the two in bipolar disorder has good clinical effect, high safety and popularization value.
[Key words] sodium valproate sustained release tablets; Quetiapine; Bipolar disorder
双相情感障碍是临床发病率较高的精神类疾病,治疗难度较大,患者主要以情绪不稳定、狂躁、抑郁等为典型症状,部分患者可与其他精神类疾病混合发作,根据临床大数据显示【1】,双相情感障碍的诱发因素包括人际关系、应激事件、家庭环境和社会环境等。现阶段双相情感障碍的治疗原则主要是控制患者的情绪【2】,目前丙戊酸钠缓释片和喹硫平是临床应用较为广泛的治疗方案,本文对二者联合治疗的临床效果进行深入分析,现做出如下阐述。
1 资料和方法
1.1一般资料
选取本院100例双相情感障碍患者作为本次的研究对象,研究对象选取时间段为2020年5月份到2021年5月份,电脑随机将所有患者均分为参照组(行单一治疗)和研究组(行联合治疗),各50例。其中参照组男性患者与女性患者的比例为30:20;最小18岁,最大55岁,平均年龄为(25.15±3.62)岁;病程在8个月-5年之间,平均病程为(3.27±0.58)年。研究组男性患者与女性患者的比例为29:21;最小19岁,最大56岁,平均年龄为(26.04±3.25)岁;病程在7个月-5年之间,平均病程为(3.78±0.35)年。经过对以上患者一般资料进行比对未发现统计学意义(P>0.05),现开展以下比较研究。
1.2方法
1.2.1参照组
本组患者予以单一治疗:予以丙戊酸钠缓释片(生产厂商:江苏恒瑞医药股份有限公司;国药准字H19991395)口服治疗,第一天500毫克,每天2次,第三天1000毫克,第四到第七天每天1500毫克到2000毫克,连续治疗三个月。
1.2.2研究组
本组患者予以联合治疗:丙戊酸钠缓释片治疗方式与上述相同,加以喹硫平(生产厂商:湖南洞庭药业股份有限公司;国药准字H20061218)治疗,第一天100毫克,一周内根据患者耐受情况增加至800毫克每天,连续治疗三个月,
1.3观察指标
对比临床效果:根据以下判定标准将治疗效果分为显效、有效和无效,其中患者病情稳定且各种临床症状改善为治疗显效,病情得到明显控制为有效,病情没有得到控制甚至恶化被视为治疗无效,有效率=(总例数-无效例数)*%。对比安全性:患者治疗后的不良反应有心动过速、头晕、便秘等,发生率越低表明治疗效果越好。
1.4 统计学分析
采用SPSS18.0软件进行统计处理,以%表示计数资料,行卡方检验,(P<0.05)时即为呈现出统计学意义。
2 结果
2.1比较两组的治疗效果
经对比分析,参照组治疗总有效率较于研究组明显较低(P<0.05)。详见表1。
表 1 两组的治疗效果对比[n(%)]
组别 | 例数 | 显效 | 有效 | 无效 | 有效率 |
研究组 | 50 | 30 | 19 | 1 | 98.00 |
参照组 | 50 | 20 | 22 | 8 | 84.00 |
| / | / | / | / | 5.983 |
P | / | / | / | / | 0.014 |
2.2比较两组不良反应
经对比分析,研究组患者出现心动过速、头晕、便秘等不良反应的人数比为0:1:1,不良反应发生率为4.00%;参照组患者出现心动过速、头晕、便秘等不良反应的人数比为3:3:3,不良反应发生率为18.00%。研究组的不良反应发生率显著低于参照组(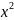 ≈5.005,P≈0.025)。
≈5.005,P≈0.025)。
3 讨论
双相情感障碍患者发病时可表现为情感高涨、精力旺盛、言语增加等狂躁症状,还可出现情绪低落、反应迟钝等抑郁症状,总之双相情感障碍患者病情复杂【3】,不同症状可同时出现,且具有不规则性、反复性、交替性、多边性等特点,给临床治疗带来了较大的难度。根据WHO调查研究结果显示【4】,世界范围内双相情感障碍的终身患病率高达2.4%,发病年龄较小,集中在18岁到25岁之间,主要发病于成人早期,女性发病率要高于男性,这主要与内分泌系统功能紊乱等因素有关,更年期、妊娠妇女的发病率要高于其它年龄段人群【5】。
本次研究采用的是两种药物联合治疗,跟单一治疗方案相比安全性更高、临床效果更好,保证治疗总有效率的同时还降低了不良反应发生率,提高预后【6】。其中丙戊酸钠缓释片作为临床常用的情感稳定剂类药物,进入人体后对多巴胺D受体和α-肾上腺素受体等进行良好的反应【7】,能够在短时间内稳定患者烦躁、抑郁、焦虑等负面情绪,具有良好的双向调节作用,从而缓解一系列精神症状,改善患者生活质量,但单一治疗临床效果有限且不良反应较多,与喹硫平联合使用可提高安全性【8】。喹硫平进入人体后可以与多巴胺D1和D2受体进行有效结合,从而稳定患者的情感,保持稳定的心态。
综上所述,二者联合治疗在双相情感障碍中临床价值更高,值得临床推广和借鉴。
参考文献
[1]张莹洁,迟勇,刘竞,等.双相情感障碍患者抑郁首发与躁狂首发的临床特点比较[J].中国医刊,2017,52(4):84-87.
[2]芹那尔·波拉提江,邹韶红.有冲动攻击行为的双相情感障碍患者与基因甲基化的研究新进展[J].神经疾病与精神卫生,2017,17(6):396-399.
[3]于海婷,周福春,薄奇静,等.临床特征与认知缺陷在双相障碍识别中的作用[J].中国医刊,2018,53(12):101-105.
[4]沙建敏,丁景景,陈光东,等.不同二联药物方案对双相情感障碍躁狂发作患者的疗效分析[J].现代实用医学,2017,29(1):115-116.
[5]刘雪峰.富马酸喹硫平片与碳酸锂联合用药方案治疗双相情感障碍躁狂发作的临床研究[J].航空航天医学杂志,2017,28(1):57-60.
[6]马建英,杨勇.富马酸喹硫平片联合碳酸锂对双相情感障碍躁狂发作患者认知功能的影响[J].检验医学与临床,2018,15(2):195-197,201.
[7]中华医学会精神病学分会.中国精神障碍分类与诊断标准第三版(精神障碍分类)[J].中华精神科杂志,2001,34(3):184-188.
[8]周焱.碳酸锂联合奥氮平治疗双相Ⅰ型障碍躁狂发作对照研究[J].临床心身疾病杂志,2017,23(3):55-57.