(兰州兰生血液制品有限公司 甘肃兰州 730046)
作者简介:房世倩,(1989.12-)本科,医学生物工程师,从事血液制品质量保证工作
通讯作者:刘晓(1984.10-),硕士研究生,副研究员,从事血液制品研究工作
摘要:目的 考察不同厂家辛酸钠对人血白蛋白产品质量的影响。方法 对两种不同厂家的辛酸钠生产的人血白蛋白分别在25±2℃和5±3℃保存0个月、1个月、2个月、3个月、6个月取样检测,进行质量可比性研究,研究的质量指标主要包括外观、可见异物检查、渗透压摩尔浓度、pH值、蛋白质含量、纯度、钠离子含量、钾离子含量、吸光度、多聚体、辛酸钠含量、铝残留量、激肽释放酶原激活剂(PKA)、无菌检查、热原检查等。结果 两种厂家辛酸钠生产的人血白蛋白各项指标均合格,A、B厂家辛酸钠生产人血白蛋白产品在25±2℃和5±3℃放置6个月后各项指标均符合要求,质量指标无显著性差异。结论 A、B厂家的辛酸钠均可应用于人血白蛋白生产。
关键词:辛酸钠;人血白蛋白;稳定性考察;质量指标
人血白蛋白是由健康人血浆经低温乙醇蛋白分离法分离纯化,并经60℃、10小时加温灭活病毒后,除菌分装而成的液体制剂。白蛋白含量96%以上,以适量辛酸钠作稳定剂,不含防腐剂和抗生素,专供静脉输注。临床上,主要用于失血性创伤以及烧伤引起休克、脑水肿以及颅内损伤引起的颅内压升高、肝硬化以及肾病引起的腹水、低蛋白血症的防治、新生儿高胆红素血症、心肺复苏术以及烧伤的辅助治疗,血液透析的辅助治疗以及呼吸窘迫综合征的治疗[1]。辛酸钠作为稳定剂广泛用于人血白蛋白的生产过程中,其在白蛋白的加热保温过程中起稳定作用,防止蛋白变性,保证制品的外观良好。
本研究对不同厂家的辛酸钠生产的人血白蛋白进行稳定性考察,进行质量可比性研究,为人血白蛋白生产用稳定剂增加合格供应商提供依据。
人血白蛋白由兰州兰生血液制品有限公司生产;A厂家辛酸钠生产的人血白蛋白批号为A1、A2、A3;B厂家辛酸钠生产的人血白蛋白批号为B1、B2、B3;辛酸钠为药用级,购自A和B厂家,批号分别为A-1、A-2、A-3和B-1、B-2、B-3,均为已批准的原辅料供应商,经备案且状态为A的供应商。
1.2设备
澄明度检测仪(型号:YB-3)购自天津博宇通达仪器有限公司;微粒分析仪(型号:GWF-8JA)购自天津天河分析仪器有限公司;冰点型渗透压仪(型号:OM819.C)购自美国ADVANCED公司;pH计(型号:Seven Excellence)购自梅特勒-托利多公司;自动定氮仪(型号:FOSS 8400)购自北京钟会达科学仪器有限公司;液相色谱仪(型号:Agilent1260)购自Agilent Technologies公司;酶联免疫测定仪(型号:MK3)购自热电上海仪器有限公司;紫外-可见分光光度计(型号:UV-1800)购自岛津制作所;无菌隔离器系统(型号:HTY-1600AG3)购自浙江泰林生物技术有限公司。
1.3方法
1.3.1A和B两个厂家辛酸钠质量可比研究
按照《中国药典》(2020年版二部)辛酸钠质量标准,分别对A和B两个厂家生产的辛酸钠进行检验,进行质量可比性研究分析。
1.3.2质量可比性研究
A厂家辛酸钠生产的人血白蛋白3批,批号为:A1、A2、A3;B厂家辛酸钠生产的人血白蛋白3批,批号为:B1、B2、B3。将A、B厂家辛酸钠生产的人血白蛋白进行质量可比性研究,考察指标为:外观、可见异物检查、渗透压摩尔浓度、pH值、蛋白质含量、纯度、钠离子含量、钾离子含量、吸光度、多聚体、辛酸钠含量、铝残留量、PKA、无菌检查、热原检查。
1.3.3稳定性考察
将两个厂家辛酸钠生产的人血白蛋白各3批分别置于25±2℃、5±3℃条件下,于0个月、1个月、2个月、3个月、6个月进行取样检测,观察纯度、多聚体、铝残留量、pH、渗透压质量指标变化趋势。
1.4质量标准及检验方法
人血白蛋白质量标准和各质量指标检验方法参照《中国药典》(2020年版三部)执行。
1.5统计学分析
所有数据采用SPSS AU软件分析进行。判定规则:P<0.05表明显著性差异,P>0.05时表明无显著性差异。
2.1 两个厂家辛酸钠质量比较
对A、B厂家生产的辛酸钠性状、鉴别、溶液澄清度与颜色、重金属、有关物质、细菌内毒素、微生物限度均符合规定。表1显示,A、B厂家辛酸钠的水分、含量、碱度指标均无显著性差异(P>0.05);微生物限度需氧菌及霉菌检测结果均为0。
表1 :A、B厂家生产的辛酸钠质量指标检测结果
厂家 | 批号 | 水分(%) | 含量(%) | 碱度 | 微生物限度(cfu/g) | |
质量标准 | ≤3 | ≥99 | 8.0-10.5 | 需氧菌≤1000 | 霉菌≤100 | |
A厂家 | A-1 | 1.2 | 100.2 | 9.5 | 0 | 0 |
A-2 | 2.5 | 100.3 | 9.4 | 0 | 0 | |
A-3 | 2.5 | 100.2 | 9.4 | 0 | 0 | |
B厂家 | B-1 | 2.7 | 99.4 | 8.9 | 0 | 0 |
B-2 | 2.8 | 99.8 | 9.4 | 0 | 0 | |
B-3 | 2.7 | 100.6 | 9.1 | 0 | 0 | |
均值 | 2.4 | 100.1 | 9.3 | 0 | 0 | |
SD | 0.6 | 0.4 | 0.2 | 0 | 0 | |
P | 0.263 | 0.445 | 0.114 | / | / | |
2.2 A、B厂家辛酸钠生产的人血白蛋白质量情况
表2显示,A、B厂家的辛酸钠生产的人血白蛋白各三批质量指标均合格,渗透压摩尔浓度、蛋白质含量、纯度、钠离子含量、铝残留量、PKA等指标均无显著性差异(P>0.05)。
表2:A、B厂家辛酸钠生产的人血白蛋白质量指标结果
检验项目 | 外观 | 可见异物检查 | 渗透压摩尔浓度(mOsmol/kg) | 不溶性微粒 | 热稳定性 | pH值 | 蛋白质含量(%) (200g/L) | 辛酸钠含量(mmol/1g蛋白质) | 纯度(%) | 钠离子含量(mmol/L) | 钾离子含量(mmol/L) | 吸光度 | 多聚体(%) | 铝残 留量 (μg/L) | 激肽释放酶原激活剂含量(PKA) (IU/ml) | 无菌检查 | 异常毒性检查 | 热原检查 | |
质量标准 | 符合规定 | 符合规定 | 210-400 | ≥10um微粒数≤6000粒容器 | 符合规定 | 6.4-7.4 | 应为标示量的95-110 | 0.140-0.180 | ≥96 | ≤160 | ≤2 | ≤0.15 | ≤5.0 | ≤200 | ≤35 | 符合规定 | 符符合规定 | 符符合规定 | |
≥25um微粒数≤600粒容器 | |||||||||||||||||||
A厂家 | A1 | 合格 | 合格 | 241 | 6,1 | 合格 | 7.0 | 101.5 | 0.164 | 96.9 | 141 | 0.1 | 0.04 | 2.4 | 15 | 2.2 | 合格 | 合格 | 合格 |
A2 | 合格 | 合格 | 240 | 7.0 | 合格 | 6.9 | 101.0 | 0.155 | 97.3 | 131 | 0.09 | 0.04 | 2.4 | 17 | 2.3 | 合格 | 合格 | 合格 | |
A3 | 合格 | 合格 | 248 | 9.1 | 合格 | 7.0 | 101.7 | 0.155 | 97.8 | 134 | 0.1 | 0.04 | 2.4 | 16 | 2.1 | 合格 | 合格 | 合格 | |
B厂家 | B1 | 合格 | 合格 | 273 | 8,0 | 合格 | 7.0 | 100.9 | 0.154 | 97 | 140 | 0.1 | 0.04 | 1.7 | 7 | 2 | 合格 | 合格 | 合格 |
B2 | 合格 | 合格 | 279 | 5,0 | 合格 | 7.0 | 101.4 | 0.152 | 97.4 | 140 | 0.1 | 0.04 | 2.3 | 21 | 2 | 合格 | 合格 | 合格 | |
B3 | 合格 | 合格 | 284 | 11,1 | 合格 | 7.0 | 100.9 | 0.151 | 97.5 | 141 | 0.1 | 0.04 | 2.2 | 9 | 1 | 合格 | 合格 | 合格 | |
均值 | / | / | 260.83 | / | / | 6.98 | 101.23 | 0.155 | 97.3 | 137.8 | 0.098 | 0.04 | 2.2 | 14.2 | 1.9 | / | / | / | |
SD | / | / | 20.03 | / | / | 0.04 | 0.34 | 0.00 | 0.33 | 4.26 | 0.00 | 0.00 | 0.27 | 5.23 | 0.47 | / | / | / | |
P | / | / | 0.636 | / | / | 0.423 | 0.279 | 0.144 | 0.917 | 0.169 | 0.423 | / | 0.214 | 0.491 | 0.249 | / | / | / | |
2.3 A、B厂家辛酸钠生产的人血白蛋白稳定性考察结果A、B厂家辛酸钠生产的人血白蛋白在25±2℃和5±3℃条件下放置0个月、1个月、2个月、3个月、6个月各项质量指标均符合质量标准,趋势稳定。
2.3.1纯度 人血白蛋白产品在25±2℃和5±3℃条件下放置0个月、1个月、2个月、3个月、6个月后,纯度均≥96%,符合质量标准要求,随着放置时间的延长在25±2℃和5±3℃条件下各批次纯度均有下降趋势。如图1所示。


图1不同温度条件下 A、B厂家辛酸钠生产的人血白蛋白纯度的趋势情况
2.3.2多聚体 人血白蛋白产品在25±2℃和5±3℃条件下放置0个月、1个月、2个月、3个月、6个月后,随着放置时间的延长在5±3℃条件下多聚体含量检测趋于平稳,在25±2℃条件下部分批次有轻微上升趋势,最终两种条件下的多聚体含量检测结果无统计学差异,均符合中国药典(2020年版三部)要求,如图2所示。


图2不同温度条件下 A、B厂家辛酸钠生产的人血白蛋白多聚体的趋势情况
2.3.3 pH值 人血白蛋白产品在25±2℃和5±3℃条件下放置0个月、1个月、2个月、3个月、6个月后,pH值均在6.4-7.4之间符合中国药典(2020年版三部)要求,随着放置时间的延长在5±3℃条件下pH值部分批次轻微下降趋势。在25±2℃条件下pH值趋势平稳,在25±2℃和5±3℃条件下的pH值检测结果无统计学差异,均符合中国药典(2020年版三部)要求,如图3所示。


图3不同温度条件下 A、B厂家辛酸钠生产的人血白蛋白pH的趋势情况
2.3.4 渗透压摩尔浓度 人血白蛋白产品在25±2℃和5±3℃条件下放置0个月、1个月、2个月、3个月、6个月后,渗透压摩尔浓度符合中国药典(2020年版三部)要求,随着放置时间的延长在5±3℃和25±2℃条件下渗透压摩尔浓度趋势平稳。在两种条件下的渗透压摩尔浓度检测结果无统计学差异,均符合中国药典(2020年版三部)要求,如图4所示。


图4不同温度条件下 A、B厂家辛酸钠生产的人血白蛋白渗透压摩尔浓度的趋势情况
2.3.5 激肽释放酶原激活剂(PKA) 人血白蛋白产品在25±2℃和5±3℃条件下放置0个月、1个月、2个月、3个月、6个月后,PKA均≤35IU/ml,符合中国药典(2020年版三部)要求,随着放置时间的延长在5±3℃和25±2℃条件下PKA趋势平稳。在两种条件下的PKA检测结果无统计学差异,均符合中国药典(2020年版三部)要求,如图5所示。
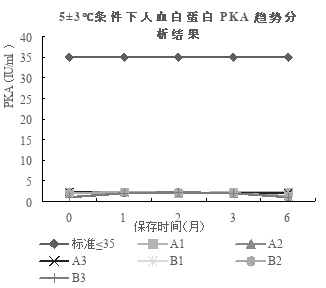

图5不同温度条件下 A、B厂家辛酸钠生产的人血白蛋白PKA的趋势情况
2.3.6 铝残留量 人血白蛋白产品在25±2℃和5±3℃条件下放置0个月、1个月、2个月、3个月、6个月后,铝残留量均≤200μg/L,符合中国药典(2020年版三部)要求,随着放置时间的延长在5±3℃和25±2℃条件下铝残留量呈缓慢上升趋势,说明铝残留量与放置时间有关,文献报道可能与药品包装材料[2]或与制品中枸橼酸离子含量有关[3]。在两种条件下的铝残留量检测结果无统计学差异,均符合中国药典(2020年版三部)要求,如图6所示。


图6不同温度条件下 A、B厂家辛酸钠生产的人血白蛋白铝残留量的趋势情况
3讨论
人血白蛋白的主要原料是健康人血浆,白蛋白是血浆中含量最多的蛋白质,约占血浆蛋白的50%-60%,人血白蛋白的药理作用主要是增加血容量和维持血浆胶体渗透压、运输及解毒、营养供给等,临床使用广泛[4]。有文献报道,白蛋白溶液的稳定性与以下两个因素有关,(1)因含有多个极性氨基酸可与水分子相互作用形成水化层;(2)白蛋白分子带有电荷。溶液中有机酸阴离子大量存在时有可能破坏白蛋白和水分子间的相互作用,降低其稳定性。由此看来,过多的辛酸钠不利于白蛋白的稳定同时有一定的毒性。资料显示,在辛酸钠浓度接近0.16mmol/g蛋白时,稳定性最好[5]。本研究以A、B厂家辛酸钠生产的人血白蛋白进行质量可比性研究。结果显示,A、B厂家辛酸钠生产的人血白蛋白各项质量指标均合格,各项质量指标无显著性差异。同时将A、B厂家辛酸钠生产的各3批人血白蛋白置于25±2℃、5±3℃,分别于0个月、1个月、2个月、3个月、6个月取样进行检测,结果显示不同温度下纯度、多聚体等项目均无显著性差异(P>0.05)。本研究采用稳定性研究方式考察了A、B厂家辛酸钠生产的人血白蛋白各项质量指标情况,结果显示均符合质量标准,两个厂家均可用于人血白蛋白的生产。
参考文献
[1]国家药典委员会.中华人民共和国药典(三部)[S].北京:中国医药出版社,2020
[2]陈宇堃,陈倩茹,邓锋,梁蔚阳.人血白蛋白中铝离子含量稳定性试验结果的探讨.中国药品标准,2019,20(4):332-338
[3]韩祥东,冯国军,袁满,赵亚宏,张俊等.人血白蛋白长期储存过程中铝残留量的研究.甘肃医药,2019,38(12):1129-1130
作者简介:房世倩,(1989.12-)本科,医学生物工程师,从事血液制品质量保证工作
通讯作者:刘晓(1984.10-),硕士研究生,副研究员,从事血液制品研究工作