作者单位:中国人民解放军联勤保障部队第九二四医院器官移植科,广西代谢性疾病研究重点实验室,广西桂林,541002
摘要
目的:研究慢病毒介导RNAi干扰技术抑制RRS1基因在胆管癌RBE细胞表达后对胆管癌RBE细胞增殖产生的影响。
方法:运用RT-PCR检测手术切除的胆管癌与癌旁胆管组织标本RRS1 mRNA基因水平的表达。通过慢病毒载体介导RNA干扰技术,从转录水平沉默RRS1基因表达,RT-PCR检测抑制RRS1后在胆管癌mRNA基因水平的表达;体外实验观察抑制RRS1基因后对胆管癌RBE细胞增殖的影响,初步探讨抑制RRS1基因表达后对胆管癌细胞增殖的影响。
结果:RT-PCR检测结果发现在胆管癌组织中的RRS1 mRNA基因表达水平较癌旁胆管组织明显升高,RNA干扰抑制RRS1基因在胆管癌RBE细胞中表达后,胆管癌RBE细胞的增殖能力受到了明显下降。
结论:1. 胆管癌组织中RRS1基因表达上调。2. 慢病毒RNAi干扰抑制RRS1基因在胆管癌RBE细胞中的表达后,RRS1会促进胆管癌细胞的增殖能力。
关键词:RRS1、胆管癌、RNA干扰、细胞增殖
ABSTRACT
Objective: To study the effect of inhibition of RRS1 gene expression by lentivirus-mediated RNAi on proliferation of cholangiocarcinoma RBE cells.
Methods: The expression of RRS1 mRNA in surgically resected cholangiocarcinoma and adjacent cholangiocarcinoma tissues was detected by RT-PCR. The expression of RRS1 gene was silenced at the transcriptional level by lentiviral vector-mediated RNA interference, and the expression of RRS1 mRNA gene in cholangiocarcinoma was detected by RT-PCR. To investigate the effect of RRS1 knockdown on the proliferation of cholangiocarcinoma RBE cells in vitro and to explore the effect of RRS1 knockdown on the proliferation of cholangiocarcinoma cells
Results:The expression of RRS1 in cholangiocarcinoma tissues is higher than those in the para-carcinoma cholangiocarcinoma tissues. Down-regulation of RRS1 aexpression can repress the proliferation of RBE cells.
Conclusion: 1. The expression of RRS1 gene was up-regulated in cholangiocarcinoma. The expression of RRS1 gene in cholangiocarcinoma RBE cells was inhibited by lentiviral RNAi interference .RRS1 promotes the proliferation of cholangiocarcinoma cells.
Key words: RRS1 Cholangiocarcinoma RNAi Proliferation
胆管癌是一类起源于胆管上皮细胞的恶性肿瘤[1],临床上较为少见。中国胆管癌患者众多,约占全世界胆管癌患者总数的55%[2],故在我国研究胆管癌有特殊的意义。但由于患者起病早期隐匿,且无特异性的肿瘤标记物及内镜诊断技术[3-4],患者就诊后多已进入肿瘤的中晚期,仅有大约10%患者适合手术治疗,术后5年生存率仅为21%-30%[5]。原癌基因的异常激活以及抑癌基因的失活已被证明为肿瘤发生的核心关键事件,了解胆管癌的致病基因有助于早期诊断和治疗。
人源RRS1(Regulator of Ribosome Synthesis 1)基因,即核糖体合成调节因子1,是一种核糖体相关蛋白,可编码人类RRS1蛋白
[6-7]。有研究结果提示人类RRS1蛋白在细胞分裂间期主要集中定位在细胞核仁,而在有丝分裂过程中则散在于染色质周围,RRS1 是一个与染色体聚集相关的核糖体蛋白,而通过RRS1 敲减的细胞,纺锤体组装的和染色体的排列表现则会出现异常,其结果将导致细胞有丝分裂的延迟[8]。已有研究表明,在多种肿瘤中均有核糖体相关蛋白的异常表达,且参与了肿瘤的发生过程,其相关机制可能为参与抑癌基因P53功能的调节[9-11]。
本研究采用RT-PCR检测RRS1在胆管癌组织及胆管癌旁组织中的表达情况,进一步应用干扰的重组慢病毒感染人胆管癌RBE细胞,观察RRS1 基因沉默对RBE细胞增殖能力影响,以期探讨其在胆管癌中的作用。
1资料与方法
1.1组织标本
本实验所选取的10例胆管癌样本组织均来源于南华大学协作医院——湖南省人民医院肝脏外科,为2013年5月至11月间手术切除的肿瘤标本,同时取相对照的10例癌旁胆管组织(距离肿瘤≥2cm)。10例胆管癌患者其中男性患者6例(60%),女性患者4例(40%);年龄43岁~70岁,中位年龄55岁;10例胆管癌样本组织病理组织分型均为腺癌,其中4例为低分化,4例中分化,2例高分化;其肿瘤解剖部位分类为:肝内型1例,肝门部5例,远端胆管4例。所有患者术前均未行任何辅助治疗,本研究获得湖南省人民医院医学伦理委员会批准。所有人组患者均签署知情同意书。
1.2主要试剂及仪器设备
SYBR Master Mixture购自Takara公司;引物(R&F)由吉凯基因完成;Oligo dT购自上海生工公司;Rnase Inhibitor、dNTPs、M-MLV 逆转录酶均购自Promega生物技术有限公司;Trizol购自invitrogen生物技术有限公司。Real time PCR 仪器(TAKARA );组织匀浆器(FLUKO);-80℃超低温冰箱(Thermo);Nanodrop 分光光度计(Thermo);高速离心机(湖南星科);台盼兮(捷倍思);DMSO(上海艾锐) ;DMEM(GIBCO) ;胰蛋白酶(上海雅心生物);Lipofectamine2000(Invitrogen);胎牛血清(上海浩然生物)荧光显微镜(上海蔡康);生物安全柜(上海博讯);Plus-20离心超滤装置(MILLIPORE);CO2培养箱(SANYO公司)。
1.3 实时荧光定量PCR检测胆管癌样本组织中RRS1的表达
使用 TRIzol 试剂( Invitrogen公司) 从样本组织细胞中提取总RNA。RNA 浓度通过 NanoDrop 2000 分光光度计( Thermo公司) 测定。根据制造商的规程,使用Oligo dT上海生工公司)、Rnase Inhibitor、dNTPs、M-MLV 逆转录酶(Promega生物技术有限公司)对 20 ~ 100 ng RNA 进行逆转录。在 LightCycler 480 系统( 上海罗氏) 上进行 qRT-PCR,并用于分析 mRNA 的表达水平。本实验采用的是在不同条件下均能稳定表达GAPDH内参基因。相对定量采用的计算方法是Ct值比较法(2-ΔΔCt法)。引物序列见表 1。
表1 RT-PCR引物设计
引物名称 | 序列信息 | 引物长度 | |
RRS1 | 上游引物 | CCCTACCGGACACCAGAGTAA | 153bp |
下游引物 | CCGAAAAGGGGTTGAAACTTCC | ||
GAPDH | 上游引物 | TGACTTCAACAGCGACACCCA | 121bp |
下游引物 | CACCCTGTTGCTGTAGCCAAA | ||
1.4 RRS1基因RNA干扰慢病毒载体的制备全流程
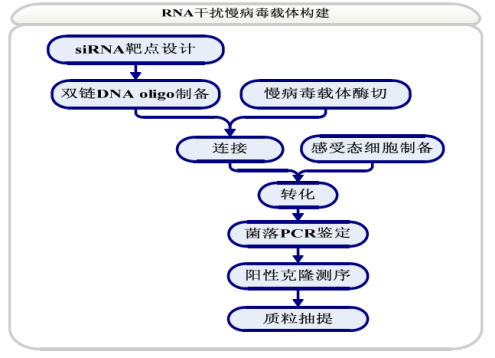
图1RRS1慢病毒载体制备流程图
1.4 RRS1-siRNA靶点序列设计及双链DNA Oligo合成
根据吉凯基因公司多年设计siRNA靶点经验以及相关设计软件,挑选出目的基因RRS1最佳动力学参数靶点进入后续实验流程(表2.1)。确认RRS1-siRNA靶点序列设计无特异性同源序列后,合成两两互补的双链DNA Oligo序列(表2.2)。
表2.1 Easy-siRNA设计序列
NO. | Accession | Target Seq | CDS | GC% |
RRS1-RNAi(13995-1) | NM_015169 | GCTGCCTTCATTGAGTTTA | 105..1202 | 42.11% |
Description | Homo sapiens RRS1 ribosome biogenesis regulator homolog (S. cerevisiae) (RRS1), mRNA. | |||
表2.2 双链DNA Oligo合成信息
NO. | 5’ | STEM | Loop | STEM | 3’ |
RRS1-RNAi(13995-1)-a | Ccgg | ccGCTGCCTTCATTGAGTTTA | CTCGAG | TAAACTCAATGAAGGCAGCgg | TTTTTg |
RRS1-RNAi(13995-1)-b | aattcaaaaa | ccGCTGCCTTCATTGAGTTTA | CTCGAG | TAAACTCAATGAAGGCAGCgg |
使用含有10%胎牛血清和DMEM(含10%FBS)的培养基中常规培养RBE细胞。传代后,在6孔板中培养RBE细胞,当汇合率到70%左右时,加入病毒,确保病毒感染效率在80%左右。RBE细胞感染慢病毒空载体为NC组,感染慢病毒 shRNA-RRS1 为 shRNA 组。
1.6 实时荧光定量PCR法检测慢病毒感染后RBE细胞中RRS1-mRNA的表达
收集成功感染后的RRS1—siRNA 组和RBE细胞转染慢病毒阴性组,用TRIzol试剂提 取2组细胞的总RNA,然后应用反转录试剂盒将RNA反转录为cDNA,以此cDNA为模板 进行实时荧光定量PCR。
1.7 Cellomics细胞计数实验检测RRS1—siRNA 慢病毒感染后RBE细胞的增殖能力
收集成功感染后的RRS1—siRNA组和RBE细胞转染慢病毒阴性组,完全培养液重悬成细胞悬液,用血球计数板计数细胞,将细胞接种于96孔板中(1 000个/孔),每组各3个复孔。分别在铺板后24h、48h、72h、96h和120 h的时间点进行Cellomics检测,并在荧光显微镜下拍照记录。通过调整Cellomics arrayscan的输人参数,准确地计算出每次扫描孔中带绿色荧光的细胞数量, 绘制细胞增殖曲线。
1.8统计学方法
采用GraphPad Prism 6.0和SPSS 24.0统 计学软件进行数据分析。所有实验均独立重3次,计量资料以x ±s表表示。2独立样本均数间的比较采用Student f检验;采用重复测量方差分析法比较各组细胞的增殖活性,组内两两比较采用 LSD—f检验。计数资料采用x²检验。P<0.05为差异有统计学意义。
2 结果
2.1 胆管癌中组织中RRS1高表达
通过实时荧光PCR检测了胆管癌样本组织与癌旁胆管样本组织,其结果(图2)发现胆管癌组织中RRS1的mRNA基因水平相对表达量是5.02±1.95,癌旁组织中RRS1的mRNA基因水平相对表达量为1.40±1.06。胆管癌样本组织中RRS1的mRNA基因表达水平较癌旁胆管组织样本明显升高,P<0.05,提示胆管癌中组织中RRS1高表达。
2.2 RRS1-siRNA抑制胆管癌RBE细胞中RRS1的表达
将含RRS1—siRNA的慢病毒组和的RBE细胞转染慢病毒阴性对照组分别感染RBE细胞后,在荧光显微镜下观察两组绿色荧光的表达情况,结果(图3)显示,从荧光结果可见目的细胞的感染率已达到80% 以上说明重组慢病毒载体-siRNA质粒已经成功转入胆管癌RBE细胞株。
将含RRS1—siRNA的慢病毒组和的RBE细胞转染慢病毒阴性对照组分别感染RBE细胞后,采用实时荧光RCR法检测胆管癌RBE细胞中RRS1 mRNA表达,结果(图4)表明经RRS1敲减后的RBE细胞组mRNA的表达水平相对表达量仅为阴性对照组的20%,数值明显低于对照组(P<0.05),评估其基因敲减效率为80.10%,提示RNA干扰抑制胆管癌RBE细胞中RRS1基因效果显著。
2.2 RNA干扰RRS1明显抑制胆管癌细胞RBE生长与增殖
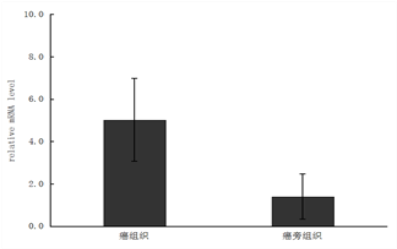
图2 两组中RRS1 mRNA的相对表达量(P<0.05)
明视野400x | 荧光视野400x | |
NC |
|
|
KD |
|
|
图3: 慢病毒感染后的RBE细胞
(NC:阴性对照组;KD:RRS1-siRNA组。)

图4 RRS1-siRNA组和对照组RRS1 mRNA相对表达量(P<0.05)
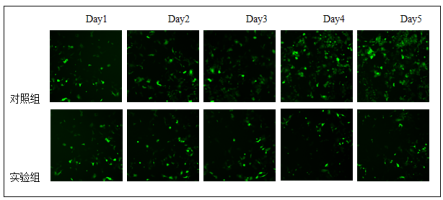
图5 慢病毒感染细胞后Cellomics细胞增殖计数
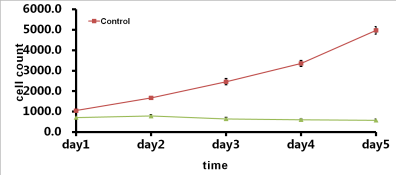
图6 RRS1-siRNA组及阴性对照组RBE细胞生长计数曲线图
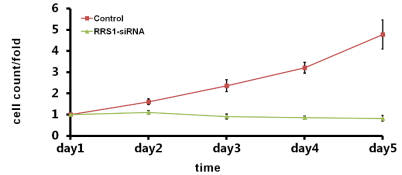
图7 RRS1-siRNA组及阴性对照组RBE细胞的增殖倍数曲线图
3 讨论
核糖体是机体蛋白质合成的重要场所,核糖体蛋白则是参与组成核糖体的主要成员,其功能作用主要是参与了蛋白质的合成[。此外,核糖体蛋白还有参与复制、转录、RNA加工、DNA修复、正常细胞恶性转化等功能,称之为核糖体外功能。当核糖体蛋白被某些危险因素(如化学性、放射性等)影响导致基因表达异常时,其结果核糖体正常功能将受损,进而产生相关连锁反应引发各种疾病,如肿瘤的发生、人类线粒体疾病等。已有大量研究表明,在多种肿瘤中有核糖体相关蛋白的异常表达(包括缺失或突变、过表达、低表达)。
根据已有文献报道,在肿瘤的发生发展中,核糖体蛋白发挥的作用机制主要包括以下几种:1、调节癌基因和抑癌基因2、调节转录和翻译3、调节细胞周期影响细胞增殖。
人源RRS1基因,即为核糖体合成调节因子1,是一种核糖体相关蛋白,其主要生理功能是在核糖体的合成过程中参与60S核糖体大亚基的装配及25S rRNA的成熟。有研究显示通过RRS1敲减的细胞,纺锤体组装的和染色体的排列表现会出现异常,其结果将导致细胞有丝分裂的延迟,提示RRS1基因可以调控细胞周期进程。研究显示,RRS1 基因在许多人类肿瘤中过表达,如甲状腺乳头状癌、肝 癌、结直肠癌、宫颈癌和乳腺癌等,并在肿瘤发生发展中起到重要作用[12-13]。我们运用了RT-PCR检测胆管癌样本组织中的RRS1mRNA基因表达水平,其结果表明胆管癌样本中RRS1基因表达水平较癌旁胆管组织显著增高,提示了在胆管癌中RRS1基因表达上调。
我们通过慢病毒介导RNA干扰技术对抑制了胆管癌RBE细胞中的RRS1基因表达。然后运用RT-PCR检测抑制RRS1表达的RBE细胞组与阴性对照组进行了mRNA基因水平表达。结果表明经抑制RRS1表达后的RBE细胞组mRNA的相对表达量仅为阴性对照组的20%,数值明显低于对照组,差异有统计学意义(P<0.05),提示RNA干扰RRS1基因效果显著。随后体外实验观察到RNA干扰抑制RRS1基因在胆管癌RBE细胞中的表达后,胆管癌细胞的增殖能力受到了抑制(P<0.05)。从而初步探讨了RRS1对胆管癌细胞生长与增殖能力影响。RRS1属于核糖体蛋白家族成员之一,而核糖体蛋白与P53的互相作用是目前研究热点之一。在大多数人类肿瘤中均有P53基因突变或活性丧失,而P53突变与胆管癌的相关性已有研究。有文献报道核糖体蛋白(包括RPL5、RPL11等)能与MDM2互相作用而抑制MDM2对P53的泛素化,从而提高P53活性,影响细胞应激反应[14]。在既往对酵母菌的研究中显示,核糖体蛋白 RPL5 和 RPL11可与 RRS1 相互作用[15]。由此,我们还推测RRS1是否通过与RPL5、RPL11互相作用,进而影响MDM2-P53信号通路,从而参与了胆管癌的发生与发展,这都需要进一步的研究与证明。
综上所述,RRS1在胆管癌组织中的阳性率明显高于胆管癌旁组织。下调RRS1基因表达可抑制癌胆管癌RBE细胞增殖。RRS1可能作为一种促癌因子参与胆管癌的发生和发展,其有望成为治疗胆管癌的新靶点。
参考文献
[1]Zeng X,Tao H.diagnostic and prognostic serum marker of cholangiocarcinoma (Reriew)[J].2015,9(1):3-8
[2]黄志强.肝胆管外科的发展方向[J].外科理论与实践,2011,16(4):329-331
[3]Malaguarnera G, Giordano M, Paladina I, et al. Markers of bile duct tumors[J].World J Gastrointest Oncol, 2011,3(4): 49-59
[4]Tamada K, Ushio J, Sugano K. Endoscopic diagno-sis of extrahepatic bile duct carcinoma: Advances and current limitations[J].World J Clin Oncol ,2011,2:203-216
[5]Friman S. Cholangiocarcinoma--current treatment options[J]. Scand J Surg, 2011,100(1): 30-34
[6]Tsuno A1, Miyoshi K, Tsujii R, etal.RRS1, a conserved essential gene, encodes a novel regulatory protein required for ribosome biogenesis in Saccharomyces cerevisiae[J]. Mol Cell Biol. 2000 Mar;20(6):2066-74.
[7]Nagase T1, Miyajima N, Tanaka A, et al. Prediction of the coding sequences of unidentified human genes. III. The coding sequences of 40 new genes (KIAA0081-KIAA0120) deduced by analysis of cDNA clones from human cell line KG-1. [J]. DNA Res. 1995;2(1):37-43.
[8]Gambe AE, Matsunaga S, Takata H, et al. A nucleolar protein RRS1 contributes to chromosome congression. FEBS Lett. 2009, 583(12):1951–1956.
[9]Zhang Y, Wang J, Yuan Y, et al. Negative regulation of HDM2 to attenuate p53 degradation by ribosomal protein L26. Nucleic Acids Res. 2010, 38, 6544-54.
[10]Dai MS, Lu H. Inhibition of MDM2-mediated p53 ubiquitination and degradation by ribosomal protein L5. J Biol Chem. 2004, 279, 44475-82.
[11]Chen D, Zhang Z, Li M, et al. Ribosomal protein S7 as a novel modulator of p53-MDM2 interaction: binding to MDM2, stabilization of p53 protein, and activation of p53 function. Oncogene. 2007, 26, 5029-37.
[12]Song JL,Hua YN,Ma ZL,et al. Effect of RRS1 gene knockdown on BT549 cell line proliferation and apoptosis in breast cancer[J].Neoplasma,2019,66( 1) : 28-32
[13]Chen F,Jin Y,Feng L,et al.RRS1 gene expression involved in the progression of papillary thyroid carcinoma[J].Cancer Cell International,2018,18( 1) : 20
[14]Krastev DB, Slabicki M, Paszkowski-Rogacz M, et al. A sys⁃tematic RNAi synthetic interaction screen reveals a link be⁃tween p53 and snoRNP assembly[J]. Nat Cell Biol, 2011,13(7):809-818.
[15]Nariai M, Tanaka T, Okada T, et al. Synergistic defect in 60S ribosomal subunit assembly caused by a mutation of Rrs1p, a ribosomal protein L11-binding protein, and 30-extension of 5S rRNA in Saccharomyces cerevisiae. Nucleic Acids Res. 2005, 33(14):4553–4562.
作者信息:
刘伟 单位: 中国人民解放军联勤保障部队第九二四医院器官移植科,广西代谢性疾病研究重点实验室,广西桂林,541002邮箱27873435@qq.com
通讯作者:赖柳生 单位: 中国人民解放军联勤保障部队第九二四医院器官移植科,广西代谢性疾病研究重点实验室,广西桂林,541002邮箱285954226@qq.com
通讯作者:赖柳生 通讯作者邮箱285954226@qq.com