中检西南计量有限公司 云南省昆明市 650000
摘要:光度测定方法是使用光度测定仪记录滴度测定过程中的光度吸收变化(即颜色变化),从而得出测定的终点,这适用于反应完全弱的系统,该系统可以用以下方法测量溶液光度测定滴滴法可用于酸碱、氧化还原、沉淀和复滴度,而复滴度滴度滴度滴度滴度滴度滴度方法则比视觉方法高,测量结果更精确。此外,这种方法的试剂利用率低,而且很容易实现自动滴定,这在某种程度上取代了劳工组织的滴定。目前,在分析化学领域还没有采用光度控制滴滴涕方法的文件系统。介绍了光度测定方法的基本原则和装置及其在食品、药品、化工等领域的应用。审查了这些标准,以便为今后在其他领域的应用提供信息,并为在该国开发基于光度测定仪的光度测定装置提供理论基础。
关键词:化学计量;滴定实验;实际问题
引言
回顾近年来全国各地高考题,化学计量的考查基本上是以物质的量为核心,将物质质量、气体体积、溶液浓度等物理量进行转化,以滴定实验为载体来确定各物质之间的量化关系.化学计量是化学实验过程中的一个必要环节,有着画龙点睛的作用.一般通过氧化还原滴定、酸碱中和滴定、沉淀滴定以及配位滴定的方法,一步或多步完成测定得到相关的数据.更为关键的是要应用化学计量关系对数据进行处理,得出正解.在解题过程中,学生要厘清实验思路,以物质的量为核心通过守恒法确定各物质之间的计量关系,再通过化学符号量化表达这种关系,得出待测物质的相关量.
一、光度滴定法
光度测定电极是一种光度测定探针,与位滴定器一起使用,可用于检测光学对比度反应的等效端点。每个光度电极探针都有发光特定波长的led灯,可将该波长的光发送到样品溶液中。在化学反应过程中,溶液的颜色会发生变化,从而导致吸收光的强度发生变化,从而转变为电子信号输出,以确定滴度的终点。使用配备光度测定电极的电位器时,通常需要在处理样品后添加一个指示器,以确定光度测定电极的最佳波长,确定该波长下的滴度,并确定终点。利用分光光度计进行了研究,以分析滴流前后的溶液,比较其光谱图,确定测量的波长,然后在这种波长条件下进行滴流实验。Muller使用传统的光度仪进行了第一次光度测定滴,使用光电探测器持续监测滴流过程中的光吸收变化,从而解决了裸眼指示器末端误差问题。随后,出现了第一个光谱仪,并增加了滴眼液的光度应用。将光谱仪改造成光度滴定仪,然后利用单片机系统形成全自动光度滴定仪,然后引导管道反应所需的反应液,在测量过程中通过调节阀门开关时间来控制流量。光度测定滴度的自动化是通过利用三路电磁阀控制滴度测定溶液来确定指示器的颜色变化来实现的。此外,还有一些科学家自制的花瓶,可用于滴灌作业,在光谱仪中添加样品和指标,在吸管下替换,滴灌用溶剂替换,终点由光吸收值或突变值确定将光谱引入滴度分析,使用钨光源提供入射光,用单色器分解,然后通过光纤传输到锥形检测瓶中。检测瓶中测试的溶液与从测定管流出的标准溶液发生化学反应,颜色发生变化。探测器检测到变化,并将圆锥形滴瓶的光信号转化为屏幕上显示的可测量的电信号,即光度吸收,从而完成滴尾监测过程。滴度测定装置使滴度测定更加精确,对外界环境的敏感性较低。随着科技的发展,微滴越来越受到关注光度滴至滴法结合了高光谱灵敏度和良好的滴至滴分析精度的优点。微滴的试剂利用率低,成本低,污染低。
二、氧化还原滴定中的指示剂
「水滴至水滴」可用作指示终点的指示器。根据指标颜色变化的原则,通常采用的氧化还原至滴度指标可分为以下几类:(1)氧化还原指标是一类物质,即使是氧化还原,其氧化状态也是如此在滴度测定过程中,随着测定剂的添加,溶液的电势不断变化,指示器被氧化或减小,以便在测量点附近从一种颜色切换到另一种颜色。(2)某些标准溶液或其标题材料甚至颜色非常深。如果测量的溶液在反应后变得无色或清晰,则在滴到滴过程中很容易检测到该试剂,因此在滴到滴过程中不需要其他指示器,并且终点可以根据被测量对象本身(称为指示器)的颜色来确定(3)特殊标志,即特殊标志,是指在本质上不氧化的物质,可以用滴滴或测量的物体产生特殊颜色,以表明滴滴的终点。
三、学以致用
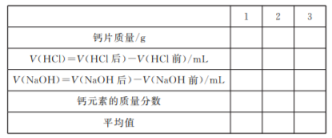
测定某品牌钙片中钙元素的质量分数.任务1:阅读材料.钙片中钙是以CaCO3的形式存在的,加工时将CaCO3研磨成极细的粉末,并辅以淀粉等材料(不含钙元素)混合均匀、压制、烘干成型.①取两片钙片称重,记录钙片质量为mg,研细后放入锥形瓶中.②记录酸式滴定管中HCl的读数,记为V1mL;向锥形瓶中加入过量的HCl标准液,不断搅拌至不再产生气体,记录滴加HCl标准液后的体积为V2mL,则V(HCl)=(V2-V1)mL.③向②的锥形瓶中滴加几滴酚酞试液.记录碱式滴定管中NaOH的读数,记为V3mL,再用NaOH标准液进行滴定至刚好出现红色,且30s后不再褪色,达到滴定终点,记录滴加NaOH标准液的体积为V4mL,则V(NaOH)=(V4-V3)mL.任务2:厘清实验方案.碳酸钙能与HCl发生反应:CaCO3+2HCl=CaCl2+CO2+H2O.过量的盐酸用标准NaOH回滴,通过与CaCO3反应的标准HCl体积求得钙片中Ca元素的质量分数.任务3:找到守恒关系.n(HCl)=2n(CaCO3)+n(NaOH),n(CaCO3)=n(Ca元素).任务4:确定计量关系.Ca元素的质量为[V(HCl)×10-3L×c(HCl)mol·L-1-V(NaOH)×10-3L×c(NaOH)mol·L-1]×40g·mol-1.Ca元素质量分数为
![]() ×100%.任务5:数据处理(如表1).
×100%.任务5:数据处理(如表1).
表1
四、配位滴定终点误差计算
坡道终点误差通常使用limbu公式计算。这种办法的优点是简单易行。但是,这种办法有以下缺点:(1)森林状况公式不是单一的通用公式,而是类似的森林状况公式。如果产权制度类型不同,林堡公式的具体形式必须单独推导出来。例如,《手册》通常给出一个用于计算单金属离子测量值的Lin bang公式,但该公式不能用于计算多金属离子总量测量值的最终误差;(limbu公式是一个近似公式,其准确性取决于滴灌终点与化学测量点之间的差异。可以看出在使用林堡公式计算结尾误差时存在着误差本身,教师在询问结尾误差的影响时很难给出明确的答案;(3)林堡公式常常被解释为,滴灌终点非常接近化学测量点,或滴灌终点接近化学测量点。这个表达有点模糊,不利于学生对学习的严格态度为解决林邦公式的上述缺陷,提出了基于分配平衡原则和结束误差体积比定义的通用分配结束误差计算方法,并给出了相应计算实例,以克服林邦公式的局限性,在该方法中发挥作用。
结束语
总之,化学计量是学习化学和解决化学问题的一种重要手段,它需要学生快速厘清实验方案,熟练运用守恒方法,准确确定计量关系,精确运用化学符号表达化学实质,从而解决化学问题.
参考文献
[1]张伟.酸碱指示剂滴定法测定碱度过程分析[J].仪器仪表与分析监测,2020(02):35-38.
[2]罗欢绵.找准计量关系,构建滴定计算解题思维模型[J].高中数理化,2020(03):69-71.
[3]杨玲.“滴定的计算”在高考中的考查[J].中学生理科应试,2020(01):47-48.
[4]吕良艳,朱其蔚.酸碱滴定过程中指示剂的选择[J].中学化学教学参考,2019(16):63-65.
[5]李国兴,李敏.构建化学的滴定理念[J].中学化学教学参考,2019(02):71-72.