广东省清远市第三中学 511500
摘 要: 氢氧化亚铁的制备是中学化学重点实验之一,由于氢氧化亚铁有比较强的还原性,极易被引入的氧气氧化生成红褐色的氢氧化铁,所以在制备氢氧化亚铁的过程对隔离氧气有较为严格的要求,本设计是针对这一要求对传统实验装置进行改进。
关键字:氢氧化亚铁;实验装置;改进
一、教材分析
本设计是针对人教版普通高中课程标准化学1(必修)第三章第二节《几种重要的金属化合物》中的一个重要实验Fe(0H)2的制备。设计一个安全、高效的化学实验不仅能够让学生亲自动手操作,增加学生探究实验的学习兴趣,还可以巩固复习Fe2+与Fe3+之间的转化关系等知识,体会Fe(0H)2制备过程中的注意事项及产生误差可能的原因,熟练掌握相关实验操作技能。
二、问题提出
教材中氢氧化亚铁的制备原理是硫酸亚铁与氢氧化钠反应,用试管作为反应器,此操作方法往往存在以下不足:由于Fe(0H)2有较强的还原性,很容易被反应物带入的空气氧化,从而导致无法长时间的观察到生成的氢氧化亚铁。针对上述问题,则需对该实验进行技术上的改进。需改进的主要问题是隔绝空气,防止空气中氧气对实验造成干扰。
三、实验装置对比
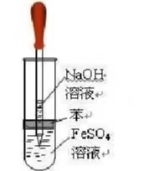
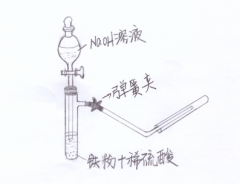
图1 教材中Fe(0H)2制备方法 图2 改进后的实验装置
四、改进实验所需仪器和药品
仪器:铁架台、具支试管、分液漏斗、弹簧夹、试管夹、带乳胶管的导管、试管、火柴
药品:还原性铁粉、稀硫酸、NaOH溶液、煤油
五、实验步骤
1.配制较浓的NaOH溶液: 将氢氧化钠(分析纯度)溶于蒸馏水配制较浓的NaOH溶液待用,采用蒸馏水配制较浓NaOH溶液可不用加热煮沸。
2.新制硫酸亚铁溶液:安装实验装置(如图2),具支试管中加入过量的还原性铁粉,接着具支试管中加入稀硫酸和煤油,最后塞上带有分液漏斗的胶塞(分液漏斗装事先准备的NaOH溶液)。
3.制备氢氧化亚铁:打开弹簧夹,待稀硫酸与还原性铁芬反应一段时间后,通过生成H2将反应器中的空气排出,最后往具支试管中加入适量的NaOH溶液,便可观察到试管中有白色絮状物生成。
六、实验原理
![]()
![]()
六、实验改进的有点及注意事项
(一)实验改进后的优点
1.改进后所需仪器及药品为常见的仪器、药品,不需特殊准备便可开展,且试剂用量较少,可节约药品且环保。
2.整个实验装置都设计在密闭容器中进行,避免了溶液与空气接触。
3.配制新制硫酸亚铁:采用的是稀硫酸与过量的还原性铁粉,利用氢气将反应器中的空气排出,且氢气具有还原性,更好地避免硫酸亚铁与氧气接触被氧化。
4.用蒸馏水配置较浓的NaOH溶液,减少了加热煮沸装置,提高了实验操作的安全性。
5.采用带弹簧夹的导管,加之里面有氢气不断溢出,减少了空气的进入,使得体系内的溶解氧达到最小程度。
6.反应生成的气体经过导管可以用向下排空气法进行收集,通过检验H2的纯度来判断反应容器中的空气是否排干净,从而达到隔绝空气,防止空气中氧气对实验的干扰,通过实践证明三天后仍可观察白色絮状物,取得了很好的实验效果。
(二)注意事项
1.进行实验时,注意检查装置的气密性。
2.本设计采用新制的硫酸亚铁溶液,久置硫酸亚铁一般会被空气氧化成 Fe3+ (4Fe(OH)₂ + O₂ + 2H₂O ==== 4Fe(OH)₃),为保证溶液中的Fe2+ 不被氧化成Fe3+,应该将新制硫酸亚铁再加点铁粉来避免Fe2+离子被氧化 (Fe +2Fe3+ =3Fe2+ )。
3.待稀硫酸与还原性铁粉反应一段时间后再滴加NaOH溶液(确保装置的空气完全排出),同时生成的氢气有还原性,为反应创造了有利的环境。
结束语
实验的改进与创新,不仅能提升教师的实验技能和创新研学精神,还可以激发学生学习热情、培养学生学科核心素养,更能实现从课堂走向课外,再从课外回归课堂的目的。
参 考 文 献
【1】赵云. 巧用具支试管改进化学实验. 化学教育2015年 第21期
【2】邢 泰 .氢氧化亚铁制备的简单化改进.中小学实验与装备2017年 第5期
![]()