上海基峰生物科技有限公司 上海市 200032
摘要:试验设计(Design of Experiments,简称DOE)是质量管理工具中一种常用的系统方法,用于规划、设计和分析科学实验,以获取准确、可靠的结果并推断因果关系。
试验设计旨在优化实验过程,帮助研究人员更有效地获取信息,探索因素之间的关系,并取得有意义的结论。该方法通过系统性地改变和控制实验中的因素,以最小化误差,获得准确的结果。
关键词:试验设计;药物研制;应用
笔者所在的生物制药领域,试验设计更具有广泛的应用,可以帮助优化生产过程、提高产品质量、减少资源浪费,并加速新药开发,应用场景可以包括:
1.培养基优化:在细胞培养过程中,培养基的成分对生物产物的产量和质量有重要影响。DOE可以帮助确定最佳的培养基配方,以最大限度地提高细胞的生长和产物产量。
2.反应条件优化:对于生物制药反应,环境条件(如温度、pH值、氧气供应等)会影响产物质量和数量。DOE可以帮助确定最佳反应条件,以获得最佳生产性能。
3.蛋白纯化工艺优化:生物制药中,蛋白质的纯化过程较为复杂。DOE可以用于优化纯化步骤的顺序、条件和参数,以提高纯度和产量,并减少杂质的存在。
4.生产线稳定性评估:在生物制药生产线中,可能会出现批次间的变异。DOE可以用于评估不同批次之间的差异,识别影响变异的因素,并制定改进措施,以实现生产的稳定性和一致性。
5.剂型优化:对于药物的剂型设计,如口服制剂、注射剂等,DOE可以帮助确定最佳的药物配方、溶剂、添加剂等,以提高药物的生物利用度、稳定性和疗效。
6.生产过程验证:在生物制药领域,生产过程的验证是必要的。DOE可以用于确定影响生产过程的关键因素,并确定合适的控制策略,确保产品质量和一致性。
7.临床试验设计:在制药研发中,临床试验的设计也可以使用DOE。通过合理的试验设计,可以确定药物剂量、试验设计、临床终点等,以最大程度地获取有关药物疗效和安全性的信息。
8.生物活性评估:在药物开发中,需要评估药物的生物活性。DOE可以用于确定最佳的实验条件和方法,以准确测量药物的生物活性。
在我司某药物研制过程中,培养基优化具有重要的意义,它直接关系到细胞的生长、产物产量和产品质量,对于生产过程的效率和产品的质量具有显著影响。因此制定DOE方案以优化培养基,具体如下。
一、设定试验目标:通过试验设计优化细胞培养基,提高细胞生长和产物产量。
二、细胞类型:研制过程中优化细菌A3的培养基,以增加其产生的蛋白质产量。
三、因素选择:在培养基优化中,选择合适的因素是非常关键的步骤,这些因素将直接影响细胞的生长、产物产量和产品质量。
我们通过对该类型细胞特性的研究,并查阅了相关文献研究、参考先前的实验经验和专家意见后,最终确定了氮源、碳源、无机盐等3个因素。
四、试验设计:我们选择使用正交表进行设计,并根据经验选取了不同因素的几个水平:氮源类型(氨酸、尿素、硝酸盐)、碳源浓度(葡萄糖 5g/L、10g/L、15g/L)以及磷酸盐浓度(0.5g/L、1g/L、1.5g/L)生成一系列试验条件。除此之外,较容易忽略的部分便是在进行表头设计时,还要考虑各因素之间可能存在的交互作用的影响,选取表头时应当避免混杂设计。因此,我们最终选择了L27(36),并将各因素及其因子置入表中,如下(表1)。
序号 | 氮源 | 碳源 浓度g/L | 磷酸盐 浓度g/L | C1-C2 | C1-C3 | C2-C3 | 序号 | 氮源 | 碳源 浓度g/L | 磷酸盐 浓度g/L | C1-C2 | C1-C3 | C2-C3 |
1 | 氨酸 | 5 | 0.5 | 1 | 1 | 1 | 15 | 尿素 | 10 | 1.5 | 2 | 3 | 3 |
2 | 氨酸 | 5 | 1 | 2 | 2 | 2 | 16 | 尿素 | 15 | 0.5 | 1 | 2 | 3 |
3 | 氨酸 | 5 | 1.5 | 3 | 3 | 3 | 17 | 尿素 | 15 | 1 | 2 | 3 | 1 |
4 | 氨酸 | 10 | 0.5 | 2 | 2 | 3 | 18 | 尿素 | 15 | 1.5 | 3 | 1 | 2 |
5 | 氨酸 | 10 | 1 | 3 | 3 | 1 | 19 | 硝酸盐 | 5 | 0.5 | 3 | 2 | 3 |
6 | 氨酸 | 10 | 1.5 | 1 | 1 | 2 | 20 | 硝酸盐 | 5 | 1 | 1 | 3 | 1 |
7 | 氨酸 | 15 | 0.5 | 3 | 3 | 2 | 21 | 硝酸盐 | 5 | 1.5 | 2 | 1 | 2 |
8 | 氨酸 | 15 | 1 | 1 | 1 | 3 | 22 | 硝酸盐 | 10 | 0.5 | 1 | 3 | 2 |
9 | 氨酸 | 15 | 1.5 | 2 | 2 | 1 | 23 | 硝酸盐 | 10 | 1 | 2 | 1 | 3 |
10 | 尿素 | 5 | 0.5 | 2 | 3 | 2 | 24 | 硝酸盐 | 10 | 1.5 | 3 | 2 | 1 |
11 | 尿素 | 5 | 1 | 3 | 1 | 3 | 25 | 硝酸盐 | 15 | 0.5 | 2 | 1 | 1 |
12 | 尿素 | 5 | 1.5 | 1 | 2 | 1 | 26 | 硝酸盐 | 15 | 1 | 3 | 2 | 2 |
13 | 尿素 | 10 | 0.5 | 3 | 1 | 1 | 27 | 硝酸盐 | 15 | 1.5 | 1 | 3 | 3 |
14 | 尿素 | 10 | 1 | 1 | 2 | 2 | |||||||
表1 正交表L27(36)
五、执行实验:在进行正式试验之前,为避免某些非预期因素的影响,将原表头的试验次序进行随机排列,并根据新的表头设计制备每个试验条件下的培养基,接种细菌并进行培养。
六、数据收集与分析:在每个试验条件下,收集细菌生长曲线、细胞密度、蛋白质产量等数据。这里以蛋白质产量为例,记录试验条件和结果如下(表2)。
Order | No | 氮源 | 碳源浓度 g/L | 磷酸盐 浓度g/L | C1-C2 | C1-C3 | C2-C3 | RES |
1 | 7 | 氨酸 | 15 | 0.5 | 3 | 3 | 2 | 55.67667 |
2 | 24 | 硝酸盐 | 10 | 1.5 | 3 | 2 | 1 | 68.96739 |
3 | 16 | 尿素 | 15 | 0.5 | 1 | 2 | 3 | 63.45186 |
4 | 8 | 氨酸 | 15 | 1 | 1 | 1 | 3 | 56.28585 |
5 | 2 | 氨酸 | 5 | 1 | 2 | 2 | 2 | 32.57906 |
6 | 22 | 硝酸盐 | 10 | 0.5 | 1 | 3 | 2 | 62.5895 |
7 | 25 | 硝酸盐 | 15 | 0.5 | 2 | 1 | 1 | 69.04613 |
8 | 21 | 硝酸盐 | 5 | 1.5 | 2 | 1 | 2 | 61.21966 |
9 | 15 | 尿素 | 10 | 1.5 | 2 | 3 | 3 | 54.6013 |
10 | 4 | 氨酸 | 10 | 0.5 | 2 | 2 | 3 | 52.07594 |
11 | 3 | 氨酸 | 5 | 1.5 | 3 | 3 | 3 | 46.87439 |
12 | 17 | 尿素 | 15 | 1 | 2 | 3 | 1 | 73.34332 |
13 | 6 | 氨酸 | 10 | 1.5 | 1 | 1 | 2 | 55.20961 |
14 | 5 | 氨酸 | 10 | 1 | 3 | 3 | 1 | 55.06029 |
15 | 11 | 尿素 | 5 | 1 | 3 | 1 | 3 | 35.70506 |
16 | 23 | 硝酸盐 | 10 | 1 | 2 | 1 | 3 | 63.72326 |
17 | 20 | 硝酸盐 | 5 | 1 | 1 | 3 | 1 | 52.0401 |
18 | 19 | 硝酸盐 | 5 | 0.5 | 3 | 2 | 3 | 50.05023 |
19 | 18 | 尿素 | 15 | 1.5 | 3 | 1 | 2 | 84.71764 |
20 | 12 | 尿素 | 5 | 1.5 | 1 | 2 | 1 | 38.91741 |
21 | 1 | 氨酸 | 5 | 0.5 | 1 | 1 | 1 | 23.25716 |
22 | 27 | 硝酸盐 | 15 | 1.5 | 1 | 3 | 3 | 75.35105 |
23 | 9 | 氨酸 | 15 | 1.5 | 2 | 2 | 1 | 57.02521 |
24 | 10 | 尿素 | 5 | 0.5 | 2 | 3 | 2 | 32.06097 |
25 | 26 | 硝酸盐 | 15 | 1 | 3 | 2 | 2 | 74.07717 |
26 | 13 | 尿素 | 10 | 0.5 | 3 | 1 | 1 | 46.77109 |
27 | 14 | 尿素 | 10 | 1 | 1 | 2 | 2 | 50.7403 |
表2 试验条件及结果
七、数据分析:使用方差分析的统计方法分析数据,确定不同因素对细菌生长和蛋白质产量的影响是否显著。结果如下。
来源 | 自由度 | Seq SS | Adj SS | Adj MS | F | P |
氮源 | 2 | 5861.5 | 5861.53 | 2930.76 | 110.06 | 0.000 |
碳源浓度 | 2 | 1134.5 | 1134.54 | 567.27 | 21.30 | 0.001 |
磷酸盐浓度 | 2 | 42.5 | 42.48 | 21.24 | 0.80 | 0.483 |
氮源*碳源浓度 | 4 | 2812.0 | 2812.02 | 703.01 | 26.40 | 0.000 |
氮源*磷酸盐浓度 | 4 | 573.5 | 573.47 | 143.37 | 5.38 | 0.021 |
碳源浓度*磷酸盐浓度 | 4 | 117.7 | 117.70 | 29.42 | 1.11 | 0.417 |
残差误差 | 8 | 213.0 | 213.03 | 26.63 | ||
合计 | 26 | 10754.8 |
通过上述结果可以看到,在本次试验中,氮源和碳源浓度这两个因子的P值都小于0.05,因此我们可以在95%的置信度下认为,这两个因子对于蛋白质产量有显著影响;相对的,磷酸盐浓度的P值为0.483,表明不显著。而在交互作用方面,氮源×碳源浓度和氮源×磷酸盐浓度这两者的交互作用P值分别为0和0.021,显示其存在一定的交互作用;碳源浓度和磷酸盐浓度之间交互作用不明显。
八、结果解释:作主效应图并结合上述数据分析的结果,进行综合评价。



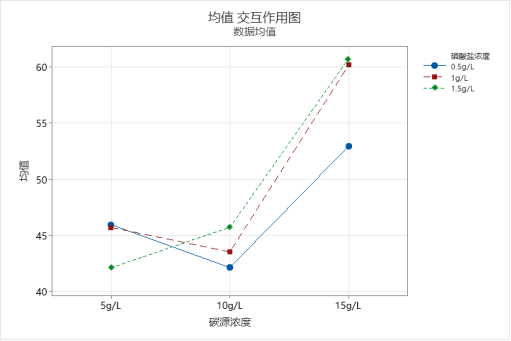
观察上列四幅主效应图,可以看出,对试验结果影响最大的因素是氮源,3个因子条件下的蛋白质产量分别为28.91、53.37、64.12,极差为35.21;其次是碳源浓度,3个因子条件下分别为44.62、43.82、57.95,极差为14.13;余下最后一个因素磷酸盐浓度对蛋白质产量的作用不明显,极差仅为2.79,基本可以忽略。而在3个因素的交互作用方面,可以看到3幅图的折线有明显交叉,显示这三者彼此之间似乎都存在一定的交互关系,但考虑到方差分析的结果,我们最终还是采信更加定量化的分析结果。
九、优化方案和验证确认:基于以上分析结果,我们确定了本次试验最佳的培养基配方,即(硝酸盐,碳源15g/L,X),对于非显著性因素硝酸盐,考虑成本、现有库存等因素,暂定1g/L。并再次使用优化后的培养基配方进行进一步的培养和验证,符合细菌生长和蛋白质产量提高的预期。
总结:作为质量管理常用工具中的试验设计,能够在更少的试验次数内获得更多有关因果关系的信息,特别在提高实验效率、降低成本、加速研究和优化过程方面,更有着无可比拟的优势。
本文通过采用试验设计的方法,通过经验选择合适的因素及因子,进行合理的试验设计和数据分析,最终达到提高细胞生长、优化产物质量、降低成本、提高生产稳定性等方面的效果。
参考资料