宁夏六盘山高级中学 宁夏 银川 750002
摘要:近年来压强平衡常数不断出现在高考题中,而课本上只介绍了平衡常数K,很多学生对于压强平衡常数Kp的计算还存在很多问题,本文设计了压强平衡常数Kp的专题学习,从认识到建构模型,再到应用模型,整个过程的学习帮助学生把握本质,突破难点。
关键词:压强平衡常数 Kp 教学设计
本文对压强平衡常数的学习主要分为以下几个环节
环节一:史话情境
通过化学史使同学们明确今天的学习内容:平衡常数。
资料:1867年,挪威化学家C.M古德贝格和P.瓦格通过大量实验发现化学反应中生成物浓度的幂之积郁反应物浓度的幂之积的比值是一个常数,我们知道这是浓度平衡常数。提出问题:![]() 浓度平衡常数表达式为?
浓度平衡常数表达式为?
学生写出该平衡常数的表达式。接着抛出问题:在近几年的高考题中都出现了压强平衡常数Kp。例如:
(2020·课标全国Ⅰ,28)将组成(物质的量分数)为2m%SO2(g)、m%O2(g)和q%N2(g)的气体通入反应器,在温度t,压强p条件下进行反应,平衡时,若SO2转化率为α,则SO3压强为 ,平衡常数Kp= (以分压表示,分压=总压×物质的量分数)
2020·课标全国Ⅱ,28 容器中通入等物质的量的乙烷和氢气,在等压(p)发生上述反应,乙烷的平衡转化率为为α,反应的平衡常数Kp= (用平衡分压代替平衡浓度来计算,分压=总压×物质的量分数)
2022·全国甲卷 金属钛(Ti)在航空航天、医疗器械等工业领域有着重要用途,目前生产钛的方法之一是将金红石(TiO2)转化为TiCl4,再进一步还原得到钛。回答下列问题:
(1) TiO2转化为TiCl4有直接氯化法和碳氯化法。在1000℃时反应的热化学方程式及其平衡常数如下:
(ⅰ)直接氯化:TiO2(s)+2Cl2(g)=TiCl4(g)+O2(g) △H1=172kJ∙mol-1,Kp1=1.0×10-2
(ⅱ)碳氯化:
TiO2(s)+2Cl2(g)+2C(s)=TiCl4(g)+2CO(g) △H2=-51kJ∙mol-1,Kp2=1.2×1012 Pa
①反应2C(s)+O2(g)=2CO(g) ![]() △H为_______kJ∙mol-1,Kp=_______。
△H为_______kJ∙mol-1,Kp=_______。
28. 硫酸亚铁在工农业生产中有许多用途,如可用作农药防治小麦黑穗病,制造磁性氧化铁、铁催化剂等。回答下列问题:
(1)在![]() 气氛中,
气氛中,![]() 的脱水热分解过程如图所示:
的脱水热分解过程如图所示:
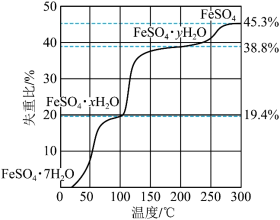
根据上述实验结果,可知![]() _______,
_______,![]() _______。
_______。
(2)已知下列热化学方程式:
![]()
![]()
![]() _______
_______![]() 。
。
(3)将![]() 置入抽空的刚性容器中,升高温度发生分解反应:
置入抽空的刚性容器中,升高温度发生分解反应:![]() (Ⅰ)。平衡时
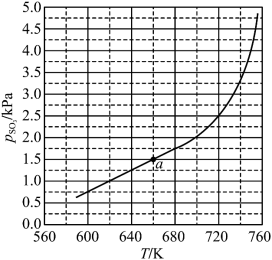
(Ⅰ)。平衡时![]() 的关系如下图所示。
的关系如下图所示。![]() 时,该反应的平衡总压
时,该反应的平衡总压![]() _______
_______![]() 、平衡常数
、平衡常数![]() _______
_______![]() 。
。![]() 随反应温度升高而_______(填“增大”“减小”或“不变”)。
随反应温度升高而_______(填“增大”“减小”或“不变”)。
提出问题,想一想:上述为高考题,实际生产过程中,对于气体参与的反应,测定气体的压强比测定气体的浓度更容易,所以我们在试题中经常会见到“Kp”,那么Kp是什么呢?引入今天的学习主题
环节二:概念认知
1.定义
有气体参与的反应,在化学平衡体系中,各气体物质的分压替代平衡浓度,计算的平衡常数叫压强平衡常数。
2.数学表达式
对于一般可逆反应mA(g)+nB(g)![]() pc(g)+qD(g),当在一定温度下达到平衡时其压强平衡常数Kp可表示为Kp=,其中p(A)、p(B)、p(C)、p(D)表示反应物和生成物的分压,用平衡分压可以这样计算:分压=总压×物质的量分数。
pc(g)+qD(g),当在一定温度下达到平衡时其压强平衡常数Kp可表示为Kp=,其中p(A)、p(B)、p(C)、p(D)表示反应物和生成物的分压,用平衡分压可以这样计算:分压=总压×物质的量分数。
p(总)=p(A)+p(B)+p(C)+p(D);==
3.计算技巧:
第一步,根据“三段式”法计算平衡体系中各物质的物质的量或物质的量浓度;
第二步,计算各气体组分的物质的量分数或体积分数;
第三步,根据分压计算公式求出各气体物质的分压,某气体的分压=气体总压强×该气体的体积分数(或物质的量分数);
第四步,根据平衡常数计算公式代入计算。例如,N2(g)+3H2(g)![]() 2NH3(g),压强平衡常数表达式为Kp=。
2NH3(g),压强平衡常数表达式为Kp=。
在化学平衡体系中,用气体物质的分压替代浓度,计算的平衡常数叫压强平衡常数。用Kp表示,"气体分压"指的是当气体混合物中的某一组分在相同温度下占据气体混合物相同的体积时,该组分所形成的压强。例如上述合成氨的反应压强平衡常数表达式为![]() 引导学生解释对于气体参加的可逆反应,为什么可以用平衡分压代替平衡浓度计算。
引导学生解释对于气体参加的可逆反应,为什么可以用平衡分压代替平衡浓度计算。
环节三:模型构建
给出题目NH4HS的分解反应为:NH4HS(S)⇋H2S(g)+NH3(g)在某一温度下把固体加入到以固定容积的容器中,反应达平衡时总压力为600KPa。求此分解反应的压强平衡常数Kp?第一步:求物质的量分数,X(H2S)=½,X(NH3)=½,第二步:求分压p(H2S)=300Kp
P(NH3)=300Kp,第三步:求Kp。举例,并创造认知冲突:一定条件下某密闭容器中存在反应2CO
2(g)+6H2(g)⇋CH3OCH3(g)+3H2O(g),若起始时容器的总压为3.6Kp,开始充入的CO2和H2的物质的量之比为1:2.6,平衡时CO2的转化率为80%,求平衡常数Kp。大家发现这个可逆反应属于前后气体分子数变化的反应,也就是随着反应的进行,气体的总压是一直变化的。对于总压的计算就有两种方法:恒容且前后气体分子数变化:![]() ,恒容且前后气体分子数不变或恒压环境:
,恒容且前后气体分子数不变或恒压环境:![]() 。由此便建构了Kp计算的模型:第一步:求平衡时各组分的物质的量,第二步:求平衡时总压,第三步:求平衡时各组分分压,第四步:根据表达式计算Kp。
。由此便建构了Kp计算的模型:第一步:求平衡时各组分的物质的量,第二步:求平衡时总压,第三步:求平衡时各组分分压,第四步:根据表达式计算Kp。
环节四:模型应用
给出相应的题目,对模型进行应用,从而掌握压强平衡常数Kp的计算方法。
例题如下:1.500 ℃时,向容积为2 L的密闭容器中通入1 mol N2和3 mol H2,模拟合成氨的反应,容器内的压强随时间的变化如下表所示,用压强表示该反应的平衡常数Kp=________
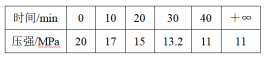
一定条件下某密闭容器中存在反应2CO2(g)+6H2(g)⇋CH3OCH3(g)+3H2O(g),若起始时容器的总压为3.6Kp,开始充入的CO2和H2的物质的量之比为1:2.6,平衡时CO2的转化率为80%,求平衡常数Kp。学生通过计算,掌握了模型,突破了Kp的计算方法。