重庆市黔江食品药品检验所,重庆 黔江 409013
摘要:目的:建立孕妇清火丸制剂中白芍药味含量测定。方法:高效液相色谱法;色谱柱:Inertsustain(4.6mm×250mm,5μm);流动相:乙腈-0.1%磷酸溶液(15:85);检测波长230nm ;流速1.0mL/min;柱温25℃。结论:本方法简便快捷、专属性强,该法中芍药苷在1.7925~1.8137mg (r=1 ,n=6)范围内进样量与对应的峰面积呈良好的线性关系,平均回收率可达(n=6) 97.28%,RSD=1.17%,初步确定孕妇清火丸制剂中芍药苷的量不得少1.80mg/g。
关键词:孕妇清火丸;高效液相色谱法;芍药苷;白芍
孕妇清火丸现收载于《中华人民国共和国卫生部药品标准》中药成方制剂第一册(WS3-B-0061-89),仅收载了处方、制法、性状及显微鉴别等项目,无控制其内在质量的标准。目前全国有2家生产企业生产销售该制剂,一是商丘市金马药业有限公司(批准文号为国药准字Z4102160 4),二是北京同仁堂制药有限公司(其批准文号是国药准字Z11020671)。为了更有效地控制该制剂质量和提高制剂使用的安全性,本次实验运用高效液相色谱法对制剂中白芍药味进行含量测定,为临床安全用药提供保障。孕妇清火丸由黄芩、知母、石斛、柴胡、地黄、薄荷、白芍、白术(麸炒)、甘草等九味药物组成,为黄褐色水丸,具有清火安胎的功效。处方中白芍温阳祛湿、补体虚、健脾胃。本制剂针对孕妇胎热有良好的疗效,具有较高的临床价值。
1 仪器与材料、试剂、试药
1.1 仪器
高效液相色谱仪(紫外-可见光检测器,SDP-20A 岛津),电子分析天平(XPE205十万分之一;XPE204电子天平;梅特勒托利多),超声波提取仪(SB-800DT,青岛海洋化工有限公司),密理博(超)纯水机(Milli Direct-Q16,美国);
1.2 试剂
乙腈、磷酸、95%乙醇(重庆万盛川东化工有限公司);水为超纯水
1.3 试药
芍药苷对照品(中国食品药品检定研究院110736-201842);孕妇清火丸(19081030,、19081035、19081034北京同仁堂制药有限公司)
2 色谱条件考察
色谱柱:以十八烷基硅烷键合硅胶为填充剂的色谱柱InertsustainC18(4.6mm×250mm,5μm);柱温:25℃;流动相:乙腈-0.1%磷酸溶液(15:85)[1-4];检测波长:230nm;流速:1.0ml/min,进样量10ul。
3 各种溶液的制备
3.1 供试品溶液的制备
取孕妇清火丸样品18g,粉碎,过3号筛。精密称取1.0g,置于具塞锥形瓶中,密塞,精密量取已经配制好的稀乙醇溶液50mL,用十万分之一的天平称定重量,超声处理60分钟(功率250W,频率33KHZ),然后放冷至室温,再次称定重量,若重量有变化就用稀乙醇补足减失的重量,然后摇匀,再用化学分析纸张和漏斗滤过,弃去前段溶液,取中间段的续滤液,然后用0.22um的微孔滤膜滤过,即得。
3.2 对照品溶液的制备
精密称取(所内编号为2021BY0172)的芍药苷对照品,加前述已经配置好的稀乙醇[5]制成每1mL含0.5mg的芍药苷对照品母液(所内编号为2021BY0172-1),摇匀,即得。
3.3 阴性对照样品溶液的制备
按照孕妇清火丸成药制剂处方除掉芍药药味,同时依照其处方比例,取阴性样品0.2g,然后按照上述供试品溶液的制备方法进行制备,得到阴性样品溶液。
4 检测波长的确定
通过试验发现白芍与芍药苷对照品经DAD检测器进行紫外吸收光谱扫描,二者均在230nm处有最大吸收,故检测波长就确定为230nm。
5方法学验证
(1)专属性试验
分别吸取3.2项下对照品溶液、3.1供试品溶液及3.3阴性样品溶液各10μL,依次注入高效液相色谱仪,上机测定,即得。
在上述2色谱条件下,芍药苷对照品峰与供试品峰保留时间相同,供试品溶液中芍药苷峰与供试品中其它组分色谱峰可达基线分离,且与其它相邻色谱峰分离度大于1.5,以及芍药苷峰的理论塔板数不得低于8000。同时对3.3阴性样品溶液进样测定时,在芍药苷峰位置处无吸收峰,即阴性无干扰。对照品、供试品、阴性样品溶液色谱峰分别见图1、图2、图3。

图1 芍药苷对照品色谱图
第1页(共30页)
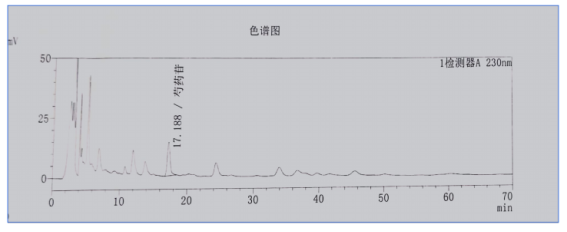
图2 孕妇清火丸供试品色谱图

图3 孕妇清火丸阴性色谱图
(2)标准曲线与线性范围考察
分别精密量取芍药苷对照品母液(浓度为0.508915mg/mL)1mL定容至50mL的具塞无色玻璃容量瓶中、精密吸取2mL母液用稀乙醇溶液定容至50mL、2mL定容至25mL、3mL定容至25mL、4mL定容至25mL,之后分别吸取上述5种不同浓度的溶液各10μL,注入高效液相色谱仪中,按上述色谱条件上机进行分析,测得峰面积结果表明,芍药苷含量在0.01018~0.08143mg范围内与峰面积呈良好的线性关系,回归方程为y = 1E+07x –6215.8,r=1。如图4、表1所示。
表1芍药苷对照品线性测定结果表
进样量C(mg) | 0.01018 | 0.02036 | 0.04071 | 0.06107 | 0.08143 |
峰面积值A | 118047 | 234437 | 489714 | 730551 | 974671 |

图4芍药苷对照品线性测定图
(3)仪器精密度试验
精密吸取对照品溶液(0.508915mg/mL)10μL,注入高效液相色谱仪中,按上述色谱条件进行分析,平行测定6次,并记录其峰面积,结果见表2:
表2 精密度试验结果
进样次数 | 1 | 2 | 3 | 4 | 5 | 6 | 平均值 | RSD |
芍药苷 峰面积A | 483900 | 480915 | 482710 | 481827 | 481082 | 480778 | 481868.7 | 0.25% |
上图显示,仪器具有良好的精密度。
(4)重复性试验
取批号为19081035的样品共6份,按前述提取方法制成供试品溶液,分别精密吸取10μL注入高效液相色谱仪,通过计算结果计算RSD值。结果见表3。
表3 方法重复性试验结果
试验号 | 1 | 2 | 3 | 4 | 5 | 6 | 平均值 | RSD |
芍药苷 含量(ug/ml) | 1.8035 | 1.8016 | 1.8024 | 1.8083 | 1.8017 | 1.8120 | 1.8049 | 0.23% |
如表3所示,样品含量平均值为1.8049ug/ml,相对标准偏差为0.23%,表明本含量测定方法具有良好的重复性。
(5)稳定性试验
1.对照品溶液稳定性试验结果
在常温条件下,取同一对照品溶液,在不改变其他参数的条件下,改变其时间参数(0h、2h、4h、6h、8h)进样取样,每次10μL,测定并记录其色谱峰面积,同时根据结果计算RSD,结果见表4。
表4对照品溶液稳定性试验结果
放置时间(h) | 0 | 2 | 4 | 6 | 8 | 平均值 | RSD |
芍药苷 峰面积值A | 444545 | 449560 | 446956 | 441891 | 449492 | 446488.8 | 0.7% |
如表4所示,供试品溶液相对标准偏差为0.7% ,表明供试品溶液在8小时内是趋于稳定的。
2.供试品溶液稳定性试验结果
在常温条件下,取同一供试品溶液,在不改变其他参数条件下,改变其时间参数(0、2、4、6、8)小时进样取样,每次10μL,测定并记录其色谱峰面积,同时根据结果计算RSD,结果见表5。
表5 供试品溶液稳定性试验结果
放置时间(h) | 0 | 2 | 4 | 6 | 8 | 平均值 | RSD | |
芍药苷 峰面积值A | 440654 | 440266 | 449848 | 448773 | 448724 | 445653 | 1.06% | |
(6)加样回收率试验
精密称取已知含量(芍药苷含量为1.8017mg/g)的样品(批号:19081035)6份,分别精密加入浓度为508.915μg/mL的芍药苷对照品母液溶液1mL,芍药苷加入量为0.001045mg,按供试品溶液的制备样品分别进样10μL,按样品测定方法测定其含量,按下述计算式计算回收率,结果见表6。
![]()
表6 芍药苷加样回收试验结果
编号 | 取样量(g) | 芍药苷 测得量(ug) | 加入芍药苷量(mg) | 回收率(%) | 平均值(%) | RSD(%) |
1 | 1.0366 | 56.245 | 0.001045 | 98.03 | 97.28 | 1.17 |
2 | 1.0421 | 56.140 | 0.001045 | 96.7 | ||
3 | 1.0788 | 57.870 | 0.001045 | 98.91 | ||
4 | 1.0802 | 57.710 | 0.001045 | 97.92 | ||
5 | 1.0018 | 54.488 | 0.001045 | 95.24 | ||
6 | 1.0057 | 54.906 | 0.001045 | 96.89 |
回收率试验结果表明,6次试验的加样回收率测得结果均在90%~99% 之间,相对标准偏差为1.17%,说明该方法的回收率良好。
5.1样品含量测定
取3(批号19081030、19081035、19081034)批不同生产批号的样品,每批取2份,按供试品溶液的制备方法制备,分别精密吸取对照品溶液10μL,样品各10μL,按前述色谱条件测定,记录色谱图,计算其含量,结果见表7。
表7 样品含量测定结果
生产批号 | 峰面积(A) | 含量(mg/ml) | 平均含量(mg/g) | RSD(%) |
19081030 | 425422 | 1.81506 | 1.8109 | 0.3 |
421181 | 1.80505 | |||
426359 | 1.81368 | |||
425074 | 1.80961 | |||
19081035 | 429406 | 1.82570 | 1.8137 | 0.5 |
424271 | 1.81113 | |||
424311 | 1.81375 | |||
424321 | 1.80419 | |||
19081034 | 423156 | 1.79643 | 1.7925 | 0.2 |
421423 | 1.79219 | |||
424486 | 1.79073 | |||
423073 | 1.79074 |
5.2 检测限
将芍药苷对照品溶液稀释,精密吸取10μL,注入高效液相色谱仪中,按上述色谱条件进行分析,测得其信噪比。最终得出检测限为10ng。
5.3 小结与结论
本试验最终确定色谱条件为色谱柱:InertsustainC18(4.6mm×250mm,5μm);流动相:乙腈-0.1%磷酸溶液(15:85);流速:1.0mL/min;柱温:25℃;进样量:10μL;检测波长:230nm。
对三批孕妇清火丸制剂中的芍药进行含量测定,试验结果每克含芍药苷1.7925~1.8137mg,暂定制剂中含芍药以芍药苷计,不得低于1.80mg/g,即不少于10.8mg/瓶。
在含量测定研究中,确定了以白芍中芍药苷作为含量测定指标。在供试品溶液的制备中,参考了《中国药典》(2020年版)[5]一部白芍药材标准项下含量测定方法。流动相经多次试验,最终选定以乙腈-0.1%磷酸溶液(15:85)为流动相,发现分离度效果良好,保留时间适宜,基线平稳,理论塔板数达到要求。
综上所述,在孕妇清火丸现有的质量标准基础上,本研究增加对白芍药味的含量测定,进一步完善了孕妇清火丸的相关质量控制标准。不足之处在于,该处方制剂成分复杂,只讨论单个药味的标准研究往往不能完全保证该制剂用药安全,所以多种药味都应建立其相应的质量标准。
参考文献:
[1]高效液相色谱法测定白芍药材中白芍总苷含量,刘敏颜,高秀强,王永等,中国药业,2008第五期:(22-23)
[2] HPLC法测定马氏接骨丸中白芍苷的含量,王旭天津市北辰中医医院制剂室
内蒙古中医药2014年 第5期:(52-52)
[3]HPLC法同时测定白芍中芍药苷、芍药苷亚硫酸酯成分含量,于定荣,谷巍等,中国中医科学院中药研究所等,海峡药学2021年5月
[4] HPLC法测定健胃胶囊中芍药苷含量,赵南、肖锦新等,贵州百灵企业集团制药股份有限公司,海峡药学2019年8月
[5] 国家药典委员会.中华人民共和国药典(一部)[S].北京:中国医药科技出版社,2020
第1页(共30页)