(海南海力制药有限公司,海南海口 570310)
摘要:阿莫西林胶囊(规格:0.25g、0.5g)由海南海力制药有限公司研发,该品种已上市,根据国家政策要求需进行仿制药一致性评价研究。拟与参比制剂Beecham Group plc的Amoxicillin Capsules阿莫西林胶囊(来源:Glaxo Welcome Production,规格250mg、500mg)进行比较,以期达到与原研产品具有质量和疗效一致性的仿制药。
关键词:阿莫西林;一致性评价;参比制剂
Abstract:Amoxicillin capsules (specification: 0.25g, 0.5g) were developed by Hainan Haili Pharmaceutical Co., Ltd. This variety has been listed. According to the national policy requirements, it is necessary to conduct a consistency evaluation study on generic drugs. It is proposed to compare it with the reference preparation Amoxicillin Capsules of Beecham Group plc (source: Glaxo Welcome Production, specification 250mg, 500mg), so as to achieve a generic drug with quality and efficacy consistency with the original product.
Key words:Amoxicillin; Consistency evaluation; Reference formulation
1 原研品简介
阿莫西林是由英国史克必成(SmithKline Beecham)公司[葛兰素威康(Glaxo Wellcome)和史克必成(SmithKline Beecham)联合,于2000年12月成立葛兰素史克公司(GlaxoSmithKline)]开发的6-氨基青霉素烷酸(6-APA)几个半合成衍生物之一,于1972年4月19日英国首次上市。
2参比制剂的处方工艺解析
经过分析,参比制剂内容物为颗粒和粉末,非活性成分只有硬脂酸镁,推测其采用的工艺为原料药干法制粒。拟评价制剂亦采用原料药干法制粒后与辅料混合均匀后直接充填胶囊的工艺,所得产品溶出行为、含量、有关物质与参比制剂相比无明显差异,关键工艺步骤包括干法制粒、总混、充填,通过对颗粒的松密度、振实密度、粒度分布、休止角、水分、混合均匀性、装量差异和溶出度等指标进行控制,确定关键工艺步骤的工艺参数。经过验证,工艺能够用于阿莫西林胶囊的连续生产,产品质量能够达到质量稳定且和参比制剂一致。
3工艺筛选
我们首选参比制剂的处方组成,研究过程中发现当处方中只有疏水性润滑剂硬脂酸镁时采用胶囊机灌装时灌装一段时间制剂在4个介质中前期溶出会变慢,尤其是在酸性介质0.1mol/L盐酸溶液和pH4.5醋酸盐缓冲液中。分析原因:由于硬脂酸镁包裹在阿莫西林表面阻滞其溶出,故在处方中加入崩解剂、助流剂,生产工艺与参比制剂一致,原料药干法制粒后加入辅料混合后直接灌胶囊。通过全面考察胶囊剂的外观性状、含量、有关物质、杂质A、聚合物、水分等指标为依据,特别是以与参比制剂的体外溶出行为作为主要对比指标,进行处方筛选。
表1 参比制剂在四种介质溶出度曲线
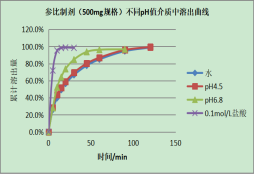

4干法制粒考察
将阿莫西林轻粉加入三维混合机混合均匀,加入干法制粒机制粒,对设备以下参数进行考察。螺旋转速(进料速度控制)、压辊转速(干法制粒速度控制)、整粒转速、工作压力、制粒筛网孔径,其中关键参数为工作压力,故以干法制粒后颗粒性状、粒度分布、水中溶出曲线为指标重点对工作压力进行考察。当工作压力60~130Bar时,4批溶出行为无明显差异。从24目~80目颗粒的收率看,工作压力在60~100Bar范围内时,颗粒收率没有明显差异,工作压力过高收率反而略有降低。
表2 干法制粒工作压力考察
批号 | 201701 | 201702 | 201703 | 201704 |
螺旋转速(rpm) | 30 | 30 | 32 | 40 |
压辊转速(rpm) | 8 | 8 | 8 | 8 |
压辊间隙(mm) | 0.5 | 0.6 | 0.6 | 0.6 |
整粒2转速(rpm) | 100 | 100 | 100 | 100 |
工作压力(bar) | 60 | 80 | 100 | 130 |
制粒筛网孔径(mm) | 0.8 | 0.8 | 0.8 | 0.8 |
压辊表面纹路 | 网纹 | 网纹 | 网纹 | 网纹 |
表3 干法制粒工作压力研究指标考察
批号 | 201701 | 201702 | 201703 | 201704 | |
是否黏辊轮 | 否 | 否 | 否 | 否 | |
性状 | 类白色颗粒 | 类白色颗粒 | 类白色颗粒 | 类白色颗粒 | |
松密度(g/ml) | 0.61 | 0.61 | 0.62 | 0.63 | |
粒度分布(%) | ≤80目 | 6.4 | 12.5 | 11.3 | 11.0 |
24-80目 | 93.6 | 87.5 | 88.7 | 89.0 | |
根据考察后的工艺参数设置制粒机参数进行中试放大,将原料阿莫西林轻粉加入干法制粒机干法制粒机中经0.8mm筛网进行制粒,制得颗粒经旋振筛20目和60目进行筛分,小于20目和大于60目的颗粒作为合格颗粒备用。加崩解剂、助流剂混合制成的胶囊与参比制剂按照质量标准项下进行溶出度曲线对比,结果一致。
表4阿莫西林胶囊中试工艺溶出度曲线


本品采用原料药干法制粒、总混、胶囊充填的制备工艺,小试研究过程中重点对干法制粒机的螺旋转速、工作压力等参数进行考察,初步确定了参数控制范围,在中试放大过程中,进一步考察和优化,并生产出合格的中试产品;在工艺验证过程中又其进一步考察和优化,进行工艺验证的生产,对各工序工艺参数的合理性进一步验证,结果表明阿莫西林胶囊生产工艺设计合理,可行性和重现性较好,满足阿莫西林胶囊连续商业化生产要求。
参考文献
[1] 阿莫西林胶囊(Amoxil®)英国上市说明书
[2] BCS Database results(tsrlinc网站的BCS分http://www.ddfint.net/search.cfm)
[3]总局关于发布仿制药参比制剂目录(第三批)的通告(2017年第65号),总局关于发布仿制药参比制剂目录(第四批)的通告(2017年第67号)
1