玉溪师范学院附属中学 云南 玉溪 653100
摘要:对于多种气体物质参加的反应,增加某一气体反应物的浓度,为什么其它反应物的平衡转化率增大,而加入的反应物本身的平衡转化率减小,用具体例题通过计算加以证明。
关键词:可逆反应;平衡移动;恒温恒容;增加;转化率
 一、转化率定义式:
一、转化率定义式:
转化率
二、再次充入气体反应物引起的转化率变化
1.反应物只有一种,再次充入反应物引起的转化率变化
此类反应为:a A(g)⇌ b B(g)+c C(g)
恒温恒容条件下,上述可逆反应达到化学平衡状态后,增加A的量,即增大了反应物的浓度。根据勒沙特列原理,平衡向正反应方向移动,但反应物A的转化率的变化与气体物质的计量数有关:
 (1)若a=b+c,则A的转化率不变;
(1)若a=b+c,则A的转化率不变;
(2)若a>b+c,则A的转化率增大;
(3)若a<b十c,则A的转化率减小。
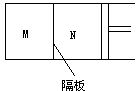
分析讨论 如图,M和N为两个等温等压容器,其中隔板固定,活塞可自由移动。
我们将m mol A充入M容器中,让其在一定温度下发生化学反应并建立化学平衡状态M1,设此时A的转化率为x%。
同温下,我们再将n mol A充入上述已达平衡状态的M容器中,由于提高了A的浓度,故化学平衡向正反应方向移动,并在恒温恒容下第二次建立化学平衡状态M2,设此时A的转化率为y%。
对于第二次n mol A的充入我们可以做这样的设置:
让n mol A先在容器N中反应,且达到化学平衡状态.我们总可以通过调整N的体积,使其与容器M为同一温度同一压强.则此时容器M和容器N中的两个化学平衡状态为等效平衡.即两容器中对应组分百分含量相等,反应物转化率也相等,且均为x%。
此时我们将隔板抽掉,压缩活塞,使容器M和N合二为一,压缩至原M容器的体积为止.此时,由于减容增压,各物质浓度均增大,正逆化学反应速率均加快,化学平衡发生移动,移动方向取决于化学方程式中气体物质的计量数。根据勒沙特列原理:
若a=b+c,平衡不移动,x=y;
若a>b+c,平衡向右移动,x<y;
若a<b+c,平衡向左移动,x>y。
例1. 一定温度下,在一定容的密闭容器中充入NO2发生如下反应:2NO2⇌N2O4并达到平衡,此时NO2的转化率为p%,再次充入NO2,其转化率将( )
A. 增大 B. 减小 C. 不变 D. 无法确定
分析:依据平衡的建立与途径无关。向平衡体系中继续充入NO2,达到的平衡与以下平衡等效:将继续充入的NO2在另一容器中建立原平衡的等效平衡和原平衡体系压缩在一起建立的平衡。由此可知,充入NO2相当于增大原平衡的压强,NO2的转化率增大。
答案:A
小结:只有一种反应物参加的可逆反应,增大反应物浓度达到新平衡,相当于增大原体系的压强,转化率的变化根据压强对平衡移动的影响来判断。
2.有两种或两种以上气体反应物参加的可逆反应
此类反应为:a A(g)+b B(g)⇌ c C(g)+d D(g)
(1)若只增加A的量,平衡正向移动,B的转化率增大,而A的转化率减小。
(2)若按原比例同倍数增加反应物A和B的量,则平衡向正反应方向移动,而反应物转化率与化学方程式中气体物质的计量数有关:
①若a+b=c+d,则A、B转化率均不变;
②若a+b>c+d,则A、B转化率均增大;
③若a+b<c+d,则A、B转化率均减小。
分析讨论 办法及过程同前。
例2. 一定温度下,在一定容的密闭容器中充入N2和H2发生反应N2+3H2 ⇌2NH3并达到平衡,N2的转化率为c%。向平衡混合物中充入N2,达到新平衡后,N2的转化率将( )
A. 增大 B. 减小 C. 不变 D. 无法确定
分析:充入N2(可用极限思想解释)平衡向正反应方向移动,H2的转化率增大,而N2的转化率却减小。
答案:B
小结:两种或两种以上反应物参加的可逆反应达到平衡后,增大一种反应物的浓度,浓度增大的物质转化率减小,其他物质的转化率增大。
例3. 一定温度下,在一定容的密闭容器中充入2molN2、3mol H2发生反应:N2+3H2 ⇌2NH3并达到平衡。若向平衡混合气体中再次充入2molN2、3mol H2,达到平衡时N2、H2的转化率将:N2,H2。(填“增大”、“减小”、“不变”或“不能确定”)
分析:同例1。N2、H2的转化率均增大。
例4. 一定温度下,在一定容密闭容器中充入2molN2、3mol H2发生反应:N2+3H2 ⇌2NH3并达到平衡。若向平衡混合气体中再次充入3molN2、3mol H2,达到平衡时N2、H2的转化率将:N2,H2。(填“增大”、“减小”、“不变”或“不能确定”)
分析:再次充入3molN2、3mol H2时,可以把3molN2、3mol H2分解为2molN
2、3mol H2和1molN2两部分,首先向原平衡混合气体中充入2molN2、3mol H2,达到平衡时N2、H2的转化率均增大(原理同例3),然后继续向该混合气体中充入1molN2达到最后平衡(原理同例2),该过程N2的转化率减小,H2的转化率继续增大,整个过程中,N2的转化率先增大后减小,所以无法确定,而H2的转化率始终增大。
小结:两种或两种以上反应物参加的可逆反应,若按起始比例充入反应物,相当于增大原平衡体系的压强;若不按起始比例充入,可把充入的反应物分解为两部分,一部分等于起始比例,另一部分是单一物质,结合例3与例2的原理综合考虑得出正确答案。
例5.对于可逆反应CO+H2O(g) ⇌CO2+H2,回答下列问题:
(1)830 K时,若起始时c(CO)=2 mol·L-1,c(H2O)=3 mol·L-1,平衡时CO的转化率为60%,水蒸气的转化率为________;平衡常数K的值为________。
(2)830 K,若只将起始时c(H2O)改为6 mol·L-1,则水蒸气的转化率为________。
(3)若830 K时,起始浓度c(CO)=a mol·L-1,c(H2O)=b mol·L-1,H2的平衡浓度c(H2)=c mol·L-1,则:
①a、b、c之间的关系式是________;
②当a=b时,a=________c。
解析:在以下计算中,各浓度单位均为mol·L-1
(1)CO + H2O(g) ⇌ CO2 + H2
起始浓度 2 3 0 0
转化浓度 1.2 1.2 1.2 1.2
平衡浓度 0.8 1.8 1.2 1.2
K==1,转化率:α(CO)=(1.2/2) ×100%=60%,α(H2O)=×100%=40%。
(2)设CO的转化浓度为x
CO + H2O(g) ⇌ CO2 + H2
起始浓度 2 6 0 0
转化浓度 x x x x
平衡浓度 2-x 6-x x x
K==1,解得x=1.5 mol·L-1,则转化率:α(CO)=(1.5/2) ×100%=75%,
α(H2O)=×100%=25%。
(3) CO + H2O(g) ⇌ CO2 + H2
起始浓度 a b 0 0
转化浓度 c c c c
平衡浓度 a-c b-c c c
K==1,化简得c=,因为a=b,所以a=2c。
答案 (1)40% 1 (2)25% (3)①c= ②2
小结:两种或两种以上气体反应物参加的可逆反应,通过计算可以得出增加一种反应物H2O的浓度,CO的转化率由60%增加到75%,H2O的转化率由40%降低到25%。
参考文献
[1] 范郴兴.用等效平衡理论判断增大反应物的用量对平衡转化率的影响.教师,2008