泰安市肿瘤防治院 271000
摘要:目的分析联合治疗方案在术后难治性复发肝癌中的临床治疗价值。方法回顾性收集并分析2016年7月至2019年3月在本院接受二联疗法与三联疗法治疗的肝癌肝切除术后难治性复发患者资料。使用改良后实体瘤疗效评价标准评估两组患者疗效,比较生存率、疾病控制率(DCR)等指标,并根据美国国立癌症研究所《不良事件常用术语标准》记录不良反应事件。结果见下面分析数据。结论PD-1抗体和TKI二联疗法及PD-1抗体、TKI和局部治疗三联疗法治疗术后难治性复发肝癌是安全有效的,后者在生存率方面有更好的临床获益。
关键词:联合治疗方案;术后;难治性复发肝癌;临床;治疗价值
引言
肝癌起病隐袭,早期诊断率低,仅20%~30%的初诊肝癌患者有机会进行根治性手术。化学药物治疗(化疗)对肝癌的疗效非常有限,分子靶向治疗药物具有一定疗效,但仍不理想。肝癌是我国肝移植的主要适应证之一,术后复发转移是影响受者长期生存的重要因素。基于此,本次探究联合治疗方案在术后难治性复发肝癌中的临床治疗价值,现报告如下。
1资料与方法
1.1一般资料
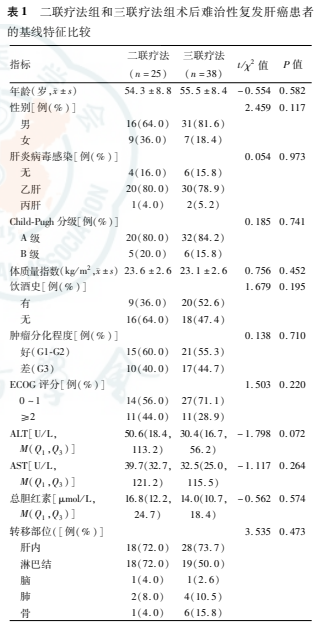
收集本院2016年7月至2019年3月诊治的63例肝癌肝切除术后难治性复发患者资料,其中男性47例,年龄(55.4士7.7)岁,女性16例,年龄(53.9+10.6)岁,包括HCC患者37例,ICC患者26例。
1.2方法
两组患者均注射治疗PD-1,每3周注射1次,或仑伐替尼,一日一次,或口服阿帕替尼,1片/次,1次/d。(2)肝内3-5个复发病灶患者行靶向治疗:方法。PD-1抑制剂。Nivolumab是一种完全人源化的单克隆抗体,可靶向结合PD-1,从而干扰免疫检查点信号传导并恢复抗肿瘤T细胞活性。CheckMate-040是一项关于Nivolumab的I/II期试验,该试验评估了Nivolumab作为晚期HCC伴或不伴慢性病毒性肝炎的单药治疗的安全性和有效性,如果患者已经进展或者不耐受一线治疗并且处于Child-PughA或B的状态,则可以准许加入其试验。此外,Pembrolizumab是另一种针对PD-1的单克隆抗体,在接受过索拉非尼治疗的晚期HCC患者的单臂II期试验(KEYNOTE-224)中进行了评估。该方法极具前景,可能是因为这两种药物的附加治疗效果可以改善肿瘤诱导的免疫抑制微环境从而产生了协同效应。CTLA-4抑制剂。Tremelimumab是一种阻断CTLA-4途径的单克隆抗体。有一项临床试验,是给予晚期HCC,Child-PughA或Child-PughB且患有慢性丙型肝炎的患者每90天接受15mg/kg的剂量。结果也值得关注,该实验RR为17.6%,DCR为76.4%,中位TTP为6.48个月,中位OS为8.2个月该试验也证实了阻断CTLA-4途径也可以有效控制肝癌的进展。(3)肝内5个复发病灶患者行TACE治疗。5F-RH导管超选至肿瘤供血动脉,对于病灶局限于肝脏某段或某叶的患者,应采取微导管进行超选择。栓塞剂选用碘化油,依据患者肿瘤的血供情况及肝功能,在透视下开始栓塞术,通过自制明胶海绵碎末强化栓塞干预。若造影显示肿瘤主干存在染色消退,则表明栓塞良好。采取肝动脉灌注化疗栓塞治疗。进行介入手术治疗前,应依据患者肝功能的实际情况对患者的肝固有动脉或肝左、右动脉进行肝动脉灌注化疗。化疗方案选取铂类+5-氟尿嘧啶+阿霉素+亚叶酸钙,灌注治疗时间不低于30min。化疗完成后,予以患者肿瘤供血动脉栓塞术,将5F-RH导管超选至肿瘤供血动脉,对于病灶局限于肝脏某段或某叶的患者,应采取微导管进行超选择。栓塞剂选用化疗药物的混合乳剂,依据患者肿瘤的血供情况及肝功能,在透视下开始栓塞术,通过自制明胶海绵碎末强化栓塞干预。若造影显示肿瘤主干存在染色消退,则表明栓塞良好。
1.3统计学方法
采用SPSS22.0对研究对象采集的数据进行分析处理,计量数据采用(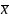 ±s)表示;计数资料采用%表示,使用χ2对数据进行校检;P>0.05为差异无统计学意义。
±s)表示;计数资料采用%表示,使用χ2对数据进行校检;P>0.05为差异无统计学意义。
2结果
2.1一般资料
本研究共纳入63例患者,其中二联疗法组25例,男性16例,女性9例,年龄(54.3土8.8)岁;三联疗法组38例,男性31例,女性7例,年龄(55.5+8.4)岁。表1为按不同疗法分组的术后难治性复发肝癌患者的基线资料,两组患者基线资料比较差异无统计学意义(P>0.05)。二联疗法组.中HCC患者12例,ICC患者13例;三联疗法组中HCC患者25例,ICC患者13例,患者按癌肿进行亚,组分析时两组患者基线特征也具有可比性。
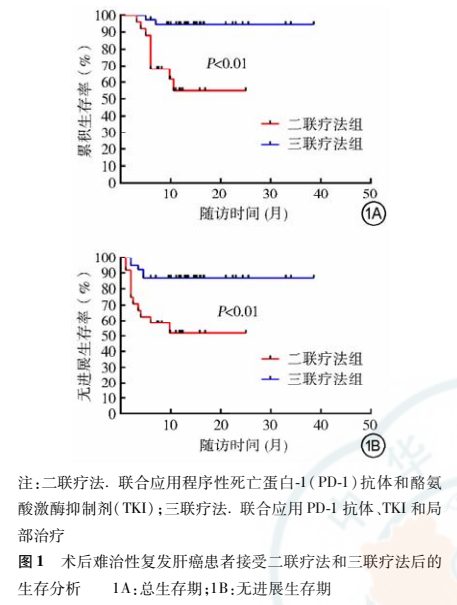
2.2患者生存情况
二联疗法组和三联疗法组的中位OS分别为7.6(6.0~11.4)个月和8.0(6.0~17.5)个月,中位PFS分别为6.0(2.0~11.4)个月和8.0(6.0~17.5)个月。二联疗法组和三联疗法组的6个月总体生存率分别为68.0%和97.4%,1年总体生存率分别为54.9%和94.5%,两组比较差异具有统计学意义(P<0.01,图1A)。二联疗法组和三联疗法组的6个月无进展生存率分别为58.3%和86.8%,1年无进展生存率分别为51.9和86.8%,两组比较差异具有统计学意义(P<0.01,图1B)。
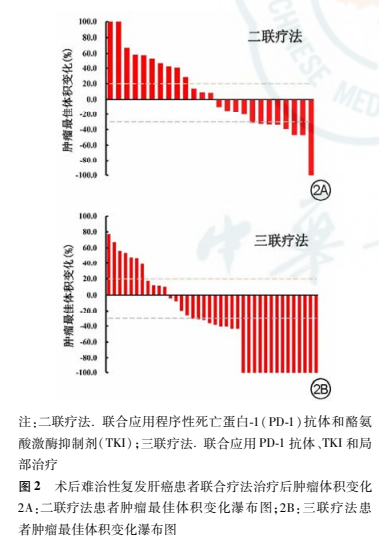
2.3肿瘤治疗反应
二联疗法组和三联疗法组的ORR分别为32.0%(8/25)和55.3%(21/38),DCR分别为64.0%(16/25)和84.2%(32/38),三联疗法组均高于二联疗法组,但两组比较差异无统计学意义(P>0.05)。如图2所示,三联疗法组中71.3%(27/38)患者和二联疗法组中48.0%(12/25患者的肿瘤体积在治疗后出现减小,肿瘤最佳体积变化的中位数分别为-36.8%(IQR,-100.0%心10.8%)和8.0%(IQR,-32.4%~49.2%)。
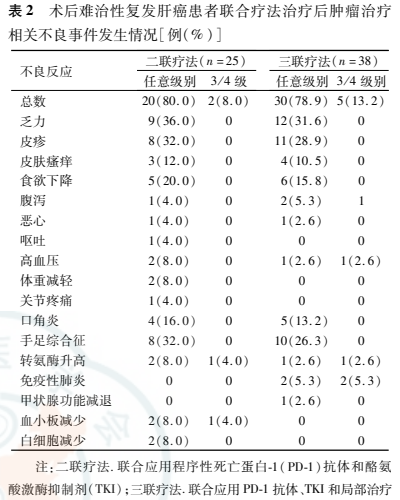
2.4治疗不良事件发生情况
在任意级别的TRAEs中,二联疗法组和三联疗法组的发生率分别为80.0%(20/25)和78.9%(30/38)(表2)。2例接受二联疗法的患者出现3/4级TRAEs(1例腹泻,1例血小板减少),而在三联疗法组中,5例患者发生了3/4级TRAEs(1例腹泻,1例高血压,1例血转氨酶升高,2例免疫性肺炎)。两组均未发生治疗相关死亡。
3讨论
肝癌术后复发的联合治疗方案经验尚浅,需严格筛选治疗方案。为了更好地治疗患者,多学科团队之间应密切合作,并研究将抗移物反应与抗肿瘤效应相分离的治疗方案。
结束语
综上所述,我们认为联合治疗方案在术后难治性复发肝癌中的临床治疗是安全有效的,值得推广和应用。
参考文献
[1]王滔.术中射频预处理在肝硬化肝癌局部切除中的临床研究[D].南昌大学,2019.
[2]亓凯,张杰,陈纯,黄绍良.静脉三氧化二砷联合化疗治疗复发难治性神经母细胞瘤7例[J].中国实用儿科杂志,2018,32(11):846-850.
[3]王海涛.TACE联合~(125)I放射性粒子植入治疗难治性肝癌的初步探讨[D].浙江大学,2018.
[4]陈秀容.HLA半相合淋巴细胞输注治疗59例难治性实体瘤的临床分析[D].福建医科大学,2018.
[5]曾普华.原发性肝癌围介入期中医证候演变规律及介入对VEGF、bFGF表达水平影响[D].广州中医药大学,2018.