武汉工程大学环境生态与生物工程学院 430205
摘要:采用凝胶过滤层析及离子交换层析联用的方法分离纯化硫酸铵盐析后的纳豆激酶,并对凝胶过滤层析分离纯化纳豆激酶的条件进行了优化研究。实验结果表明在硫酸铵饱和度为30%,柱直径为20mm,PH值为6.4,缓冲液流速为2.0 mL/min,离子强度为0.05 mol/L时,经凝胶过滤层析及离子交换层析后,能得到纯度较高的纳豆激酶,纯化倍数为7.16倍,回收率为70.13%。本研究在柱层析法分离纯化纳豆激酶的条件优化方面可为纳豆激酶生产的工业化提供参考。
关键词:纳豆激酶;分离纯化;凝胶过滤柱层析;离子交换柱层析;条件优化
引言:纳豆激酶(Nattokinase,NK)是在纳豆发酵过程中由枯草芽孢杆菌产生的一种具有强力纤溶活性的碱性丝氨酸蛋白酶[1]。大量实验证明,纳豆激酶具有显著的溶栓活性[2],并且与目前已广泛应用的溶栓药物相比,纳豆激酶具备更多的优点,因此纳豆激酶极有可能成为更具竞争力的溶栓药物。目前工业化生产纳豆激酶主要通过分离纯化纳豆芽孢杆菌的发酵液提取[3]。从纳豆激酶被发现起,已有不少对其分离纯化的研究[4],但目前少有高纯度的纳豆激酶能被大量生产。柱层析法在纳豆激酶的分离纯化方面[5]应用广泛,由于亲和层析与疏水层析大量分离纯化纳豆激酶所需的成本过高,不适合作为工业化生产纳豆激酶的工艺。本研究通过凝胶过滤柱层析及离子交换柱层析联用的方法分离纯化硫酸铵盐析后的纳豆激酶,通过对柱层析法分离纯化纳豆激酶的条件优化为纳豆激酶的进一步工业化生产提供思路。
1 实验部分
1.1 菌株
本实验室构建并保藏的菌株枯草芽孢杆菌突变菌株YC4(Bacillus subtilis YC4)。
1.2 实验方法
1.2.1 粗酶液的制备及柱层析前处理
通过摇瓶发酵得到粗纳豆激酶发酵液,并于8500r/min离心30min,除去菌株沉淀,取上清液进行硫酸铵盐析,用纤维蛋白平板法测定纳豆激酶酶活,用考马斯亮蓝法进行蛋白质含量测定。
1.2.2 凝胶过滤层析分离纯化纳豆激酶
采用SephadexG-50作为凝胶过滤层析介质,柱长为30cm的层析柱,通过单因素试验对凝胶过滤层析过程中的脱盐与否、柱直径、pH值、流速、离子强度进行优化。
1.2.3 离子交换层析分离纯化纳豆激酶
通过离子交换层析对凝胶过滤层析后的样品溶液进行分离纯化,采用CM-Sepharose Fast Flow作为离子交换层析介质,尺寸为Φ2.0×20cm的层析柱,洗脱方式为梯度洗脱。
2 实验结果与分析
2.1 硫酸铵盐析曲线
由图2-1可知,随着硫酸铵饱和度的增加纳豆激酶逐渐从上清液转移到沉淀中。本研究中选择饱和度为30%的硫酸铵对纳豆激酶粗酶液进行盐析。
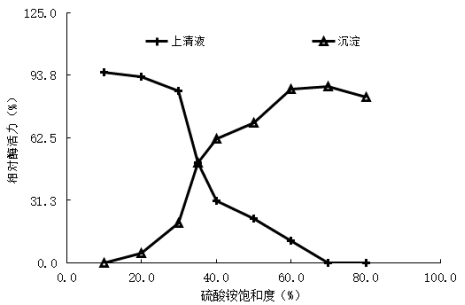
图2-1 纳豆激酶盐析曲线图
Fig.2-1 Nattokinase salting-out curve
2.2 单因素优化实验结果
过柱前是否脱盐对分离效果的影响:在进行凝胶过滤柱层析之前先脱盐处理的纯化倍数和酶活回收率均更高,即分离纯化效果更好。由于本实验选择的葡聚糖凝胶G50具有一定的脱盐作用,会在过柱时对未进行脱盐处理的样品进行脱盐。由于过柱前脱盐需要进行透析这一步骤,使得分离纯化耗费时间更长,并且会导致分离纯化的成本增加,所以这一处理并不是必要的步骤,为了使操作更简便、经济,可以省去。
柱直径对分离效果的影响:实验结果表明当柱直径为20mm时,纳豆激酶的酶活回收率和纯化倍数最高。但这并不代表柱直径越大,分离纯化效果越好。可能是由于柱直径的变化导致柱床体积的变化或者是柱直径偏小造成了管壁效应,导致分离纯化效果不好。
PH值对效果的影响:实验结果表明当缓冲盐溶液pH为6.4时,凝胶过滤柱层析法分离纯化纳豆激酶的效果最好。
流速对分离效果的影响:实验结果表明不同流速对酶活回收率以及纯化倍数的影响都很小,即一定流速范围内不同流速对分离纯化的影响很小。本试验中凝胶过滤层析法分离纯化纳豆激酶的最优流速为2.0 mL/min。
离子强度对分离效果的影响:实验结果表明当离子强度为0.05mol/L时,纯化倍数和酶活回收率均最高,即当离子强度为0.05mol/L时,分离纯化效果最好。
2.7 纳豆激酶分离纯化结果
纳豆激酶分离纯化中每一步的效率如表1。经过一系列纳豆激酶分离纯化步骤后,能得到单一的电泳条带(27.7kd),与各文献中纳豆激酶的分子大小相符合。
本次研究得到了更高纯度的纳豆激酶并减少了分离纯化过程中的酶活损失,但本方法尤其适用于实验室规模制备高纯度的纳豆激酶,不宜直接放大并大规模分离纯化纳豆激酶国内生产纳豆激酶的技术工艺仍处于初级阶段,我国目前也仅开发了纳豆保健品的生产,而对柱层析法分离纯化纳豆激酶的条件优化研究能使大量高纯度的纳豆激酶产品的生产指日可待。
表1纳豆激酶分离纯化结果
Fig.1 Nattokinase isolation and purification results
样品 | 总酶活力 (IU) | 总蛋白含量 (mg) | 比酶活 (IU/mg) | 回收率 (%) | 纯化倍数 |
发酵上清液 | 325928.62 | 6.84 | 47650.38 | 100 | 1 |
硫酸铵盐析后 | 272639.29 | 3.76 | 72510.45 | 83.65% | 1.52 |
凝胶过滤柱层后 | 245773.85 | 1.32 | 186192.31 | 75.41% | 3.91 |
离子交换层析后 | 231847.24 | 0.68 | 340948.80 | 70.13% | 7.16 |
参考文献
[1] Weng Y, Yao J, Sawyer S. et al. Nattokinase: an oral antithrombotic agent for the prevention of cardiovascular disease[J]. International Journal of Molecular Sciences, 2017, 18(03):523-536
[2] Hong J, McGowan M, Ren N, et al. Nattokinase: a promising alternativeinprevention and treatment of cardiovascular diseases[J]. Biomarker Insights, 2018, 13(10): 1177-1181
[3] Pan X, Liang P, Teng L, et al. Study on molecular mechanisms of nattokinase in pharmacological action based on label-free liquid chromatography-tandem mass spectrometry[J]. Food Science and Nutrition, 2019, 12(10):3185-3193
[4] Guo H, Ban Y H, Cha Y, et al. Comparative anti-thrombotic activity and haemorrhagic adverse effect of nattokinase and tissue-type plasminogen activator[J]. Food Science and Biotechnology, 2019, 28(5):1535-1542
[5] Fa Y, Zhang J, Zhao H, et al. Progress in separation and purification of nattokinase and its enzyme activity determination[J]. Institute of Bioenergy and Bioprocess Technology, 2019, 37(03):274-278